Bakrena sulfidna struktura, lastnosti, uporablja

- 1575
- 51
- Miguel Gutmann DVM
On bakreni sulfid Je družina anorganskih spojin, katerih splošna kemična formula je CuxSin. Ja x Je večje od in Pomeni, da je ta sulfid bogatejši v bakra kot v žveplom; in če nasprotno, x Je manjši od in, Potem je sulfid bogatejši v žveplom kot v bakra.
V naravi prevladujejo številni minerali, ki predstavljajo naravne vire te spojine. Skoraj vsi so bogatejši v bakra kot v žveplom, njihova sestava pa je izražena in poenostavljena s formulo zxS; tukaj x Lahko celo vzamete delne vrednosti, kar kaže na stehiometrično trdno snov (CU1.75Na primer).
 Vzorec minerala Covellita, enega od številnih naravnih virov bakrenega sulfida. Vir: James St. John [cc do 2.0 (https: // creativeCommons.Org/licence/by/2.0)]
Vzorec minerala Covellita, enega od številnih naravnih virov bakrenega sulfida. Vir: James St. John [cc do 2.0 (https: // creativeCommons.Org/licence/by/2.0)] Čeprav je v osnovnem stanju žveplo rumeno, njegove izpeljane spojine izgledajo temne barve; Takšno se pojavlja tudi z bakrenim sulfidom. Vendar pa mineral Covelita (vrhunska slika), ki je v glavnem sestavljen iz CU -jev, kaže kovinska bleščica in modrikasto iridescenco.
Pripravijo jih lahko iz različnih virov bakra in žvepla, z uporabo različnih tehnik in spreminjanjem sinteznih parametrov. Tako lahko dobite nanodelce z zanimivimi morfologijami.
[TOC]
Struktura bakrene sulfida
Povezave
Ta spojina ima videz kristalnega, zato lahko takoj pomislite, da je sestavljena iz Cu ionov+ (Monovalentni baker), Cu2+ (Dvovalentni baker), s2- E, tudi, s2- in s22- (disulfur anioni), ki delujejo prek elektrostatičnih sil ali ionske vezi.
Vendar pa obstaja rahel kovalenten značaj med Cu in S, zato povezave Cu-S ni mogoče izključiti. Iz tega sklepanja se kristalna struktura CUS (in vseh izpeljanih trdnih snovi) začne razlikovati od tistih, ki jih najdemo ali označujemo za druge ionske ali kovalentne spojine.
Z drugimi besedami, o čistih ionih se ni mogoče pogovarjati, toda sredi njenih znamenitosti (kation-anion) se rahlo prekriva njene zunanje orbitale (deljenje elektronov).
Koordinacije v Coveliti
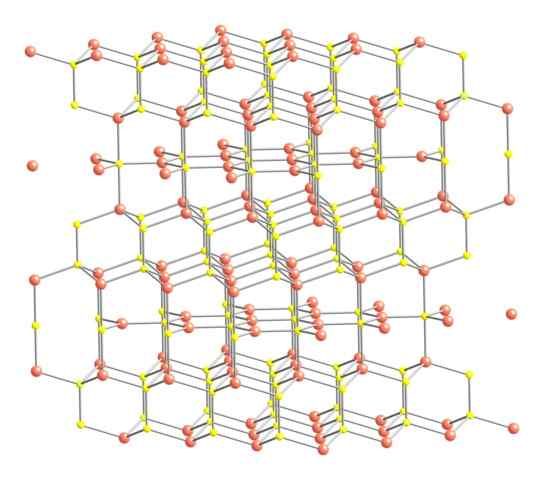 Kristalna struktura Covellita. Vir: Benjah-BMM27 [javna domena].
Kristalna struktura Covellita. Vir: Benjah-BMM27 [javna domena]. Po navedbah je kristalna struktura kovelita prikazana na sliki. Sestavljen je iz šestkotnih kristalov (opredeljen s parametri njihovih enotnih celic), kjer se ioni vežejo in vodijo v različnih koordinacijah; To so, z raznolikim številom bližnjih sosedov.
Vam lahko služi: vrsta povezave 02Na sliki so bakreni ioni predstavljeni z roza kroglami, medtem ko žveplo z rumenimi kroglami.
Najprej se osredotoča na roza sfere, opazimo, da so nekatere obkrožene s tremi rumenimi sferami (trigonalna ravna koordinacija), druge pa za štiri (tetraedrska koordinacija).
Prvo vrsto bakra, trigonalne, je mogoče prepoznati v ravninah, pravokotne na šesterokotne obraze, ki jih dajejo do bralca, v katerem so druga vrsta ogljika, tetraedra.
Zdaj se udeležujejo rumenih kroglic, nekatere imajo pet roza kroglic (trigonalna koordinacija bipiramid) in še tri in rumeno kroglo (spet tetraedrska koordinacija); V slednjem je pred disulfidnim anionom, ki ga je mogoče vizualizirati navzdol in znotraj iste strukture kovelita:
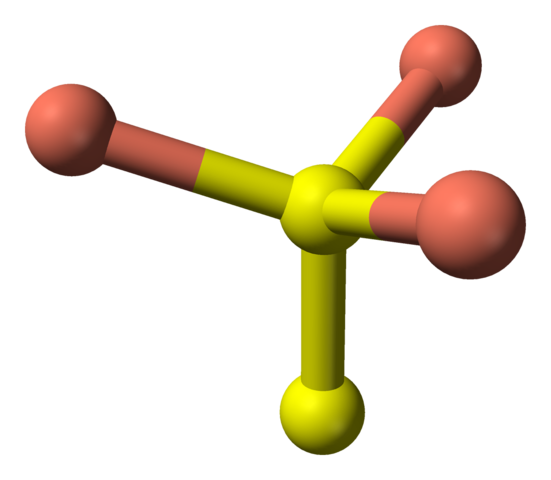 Tetraedrska koordinacija disulfidnega aniona v Covelliti. Vir: Benjah-BMM27 [javna domena].
Tetraedrska koordinacija disulfidnega aniona v Covelliti. Vir: Benjah-BMM27 [javna domena]. Alternativna formula
Takrat obstajajo Cu ioni2+, Cu+, S2- in s22-. Vendar pa študije, izvedene s fotoelektronsko spektroskopijo XPS (XPS), poudarjajo, da je ves baker kot kationi Cu+; In zato je začetna formula CUS izražena "boljša" kot (Cu+)3(S2−) (S2)-.
Opazite, da je razmerje Cu: s za prejšnjo formulo še naprej 1, prav tako pa se obremenitve prekličejo.
Drugi kristali
Bakreni sulfid lahko sprejme ortorrombične kristale, kot v polimorfu, γ-Cu2S, kalkocita; Kubični, kot v drugem polimorfu kalcita, α-Cu2S; Tetragonalni, v mineralu Anilita, Cu1.75S; monoklinic, v Djurleita, Cu1.96S, med drugim.
Za vsako definirano steklo je mineral, vsak mineral pa ima svoje lastnosti in lastnosti.
Lastnosti
Splošno
Lastnosti bakrenega sulfida so podvržene razmerja Cu: s trdne snovi. Na primer tisti, ki predstavljajo anione22- Imajo šesterokotne strukture in so lahko polprevodniki ali kovinski vodniki.
Vam lahko služi: kalijev fosfat (K3PO4): struktura, lastnosti, uporabeČe je vsebina žvepla sestavljena iz anionov2-, Sulfidi se obnašajo kot polprevodniki in predstavljajo tudi ionske prevodnosti pri visokih temperaturah. To je zato, ker njihovi ioni začnejo vibrirati in se premikati znotraj kristalov, s čimer prevažajo električne naboje.
Optično, čeprav je odvisen tudi od njegove sestave bakra in žvepla, lahko sulfidi ali ne absorbirajo sevanje v infrardečem območju elektromagnetnega spektra. Te optične in električne lastnosti omogočajo izvajanje potencialnih materialov v različnih napravah.
Druge spremenljivke, ki jih je treba upoštevati, poleg Cu Odnos: S, je velikost kristalov. Ne samo, da gre za več "žveplov" ali "koplje" bakrene sulfide, ampak dimenzije njihovih kristalov dajejo netočen učinek na njihove lastnosti; Tako se znanstveniki želijo učiti in iskati aplikacije za nanodelce CUxSin.
Covelita
Vsak mineralni ali bakreni sulfid ima edinstvene lastnosti. Vendar je od vseh Covelita najbolj zanimiva z strukturnega in estetskega vidika (zaradi svoje iridescence in modrih tonov). Zato so nekatere njegove lastnosti omenjene spodaj.
Molarna masa
95.611 g/mol.
Gostota
4,76 g/ml.
Tališče
500 ° C; Toda pokvari se.
Topnost vode
3.3 · 10-5 G/100 ml pri 18 ° C.
Prijave
Nanodelci v medicini
Ne samo da spreminja velikost delcev do dosega. Tako lahko bakreni sulfid tvori nanosfer, palice, krožnike, tanke filme, kletke, kable ali cevi.
Ti delci in njihove privlačne morfologije pridobivajo individualne aplikacije v različnih medicinskih deželah.
Nanojaule ali prazne sfere lahko na primer služijo kot prevozniki drog znotraj telesa. Nanosferas so bili uporabljeni, podprti z ogljikovim steklom in ogljikovimi nanocevkami, ki služijo kot detektorji glukoze; kot tudi njihovi agregati so občutljivi na odkrivanje biomolekul, kot je DNK.
Lahko vam služi: 6 naravnih kazalnikov pH in njihove značilnostiNanocevke Cus presegajo nanosfere pri odkrivanju glukoze. Poleg teh biomolekul so bili imunosenzorji zasnovani iz tankih filmov CUS in nekaterih podpor za patogeno odkrivanje.
Nanokristali in amorfni agregati CU -jev lahko celo povzročijo apoptozo rakavih celic, ne da bi povzročili poškodbe zdravih celic.
Nanoznanost
V sprednjem subsekciji je bilo rečeno, da so bili njihovi nanodelci del biosenzorjev in elektrod. Poleg takšnih načinov so znanstveniki in tehniki izkoristili tudi svoje lastnosti za oblikovanje sončnih celic, kondenzatorjev, litijevih baterij in katalizatorjev za zelo specifične organske reakcije; nepogrešljivi elementi v nanoznanosti.
Prav tako je treba omeniti, da se je set NPCUS-CA (CA: Actived Carbon in NP: nanodelci), ko so podprti na aktiviranem ogljiku Viri iz virov vode, ki absorbirajo neželene molekule.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Wikipedija. (2019). Bakreni sulfid. Pridobljeno iz: v.Wikipedija.org
- Ivan Grozdanov in metodija Najdoski. (devetnajst devetdeset pet). Optične in električne lastnosti bakrenih sulfidnih filmov spremenljive sestave. Časopis za trdno državno kemijo zvezek 114, številka 2, 1. februar 1995, strani 469-475. doi.org/10.1006/jssc.Devetnajst devetdeset pet.1070
- Nacionalni center za informacije o biotehnologiji. (2019). Bakreni sulfid (CUS). Baza podatkov Pubchem. Cid = 14831. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Peter a. Ajibade in nandipha l. Botha. (2017). Sinteze, optične in strukturne lastnosti
- bakrenih sulfidnih nanokristalov iz predhodnikov posameznih molekul. Oddelek za kemijo, Univerza v Fort Hare, zasebna torba X1314, Alice 5700, Južna Afrika. Nanomateriali, 7, 32.
- Sodelovanje: Avtorji in uredniki zvezkov III/17E-17F-41C.F.). Bakreni sulfidi (Cu2s, Cu (2-X) s) kristalna struktura, parametri latice. V: Madelung oz., Rössler u., Schulz m. (ur.) Netetraedralno vezani elementi in binarne spojine i. Kondenzirana snov Landolt-Börnstein-Group III (Numerični podatki in funkcionalni odnosi v znanosti in tehnologiji), Vol 41C. Springer, Berlin, Heidelberg.
- Momtan, f., Vafaei, a., Ghaedi, m. et al. Korejski J. Kem. Eng. (2018). Uporaba bakrenih sulfidnih nanodelcev, naloženih z aktiviranim ogljikom za hkratno adsorpcijo termirnih barvil: metodologija odzivne površine. 35: 1108. doi.org/10.1007/S11814-018-0012-1
- Goel, s., Chen, f., & Cai, w. (2014). Sinteza in biomedicinska uporaba nanodelcev bakrenega sulfida: od senzorjev do teranostike. Majhna (Weinheim der Bergstrasse, Nemčija), 10 (4), 631-645. Doi: 10.1002/SMLL.201301174

