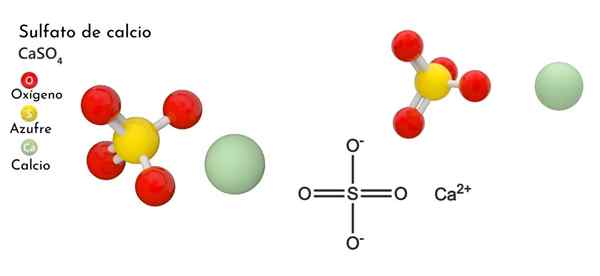
Kemična struktura, lastnosti kalcijevega sulfata (Case4), uporabe
- 2847
- 427
- Raymond Moen
Kaj je kalcijev sulfat?
On Kalcijev sulfat To je trinarna sol kalcija, alkalinoko (MR. Scholambara), žveplo in kisik. Njegova kemična formula je primer4, Kar pomeni, da za vsako kation ca2+ Obstaja anion42- interakcijo s tem. Predstavlja spojino s široko porazdelitvijo v naravi.
Njegove najpogostejše oblike so tako4· 2H2Ali (omet) in primer brezvodne oblike4 (Anhidrit). Obstaja tudi tretja oblika: omet ali omet Pariza, ki ga proizvaja ogrevanje omet (ohišje hemidrata4· 1/2h2Da).
Kalcijev sulfat je zelo uporabna spojina pri delu človeka, saj se uporablja v številnih funkcijah, ki vključujejo gradnjo cest, okrasitev doma in celo popravilo kosti.
Kemična struktura kalcijevega sulfata

Na zgornji sliki je za primer prikazana ortorrombična enotna celica4. Tu se domneva, da so interakcije izključno elektrostatične; to pomeni, da ta kationi2+ Tako privabljajo tetraedrske anione42-.
Vendar pa CA2+ Zelo je nagnjeno k koordinaciji, ki tvori poliedrske strukture okoli njega. Kaj je to? Do elektronske razpoložljivosti kalcija, da sprejme elektrone osnovnih ali negativnih vrst (na primer atomi O42-).
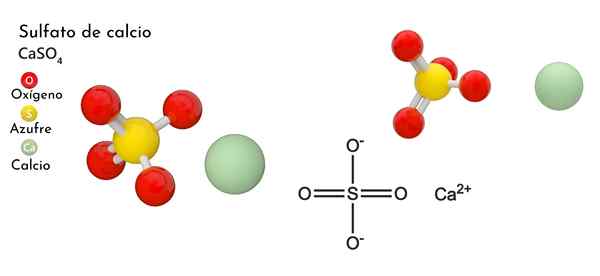
Glede na prejšnjo točko, zdaj CA ioni2+ Sprejemajo dativne povezave (ki jih zagotavlja O) in enotna celica se preoblikuje, kot kaže spodnja slika:
Posledično nastane poliedro Cao8 (Zelena sfera Ca2+ obkrožene z osmimi rdečimi sferami ali tetraedri4 blizu). Kalcijevi poliedroni in sulfatni tetraedri; To je kristalna struktura primera4 brezvodna.
Lahko vam služi: bipe beraral: kaj je, značilnosti, za kaj jePoleg tega, ko so kristali hidrirani -oblikovanje di -hidrirane soli ali hemidrata (primer4· 1/2 h2O)- struktura se zamuja, da vključi molekule vode.
Te molekule je mogoče prepletati in uskladiti s kalcijam; to pomeni, da nadomestijo eno ali dve skupini sulfata.
Po drugi strani pa ne gre vsa voda za integracijo Cao Polyhedron8. Nekateri po drugi strani tvorijo vodikove mostove s sulfati. Ti služijo kot zveza za dva odseka v cikcagu, izdelki razporeditve ionov v steklu.
Lastnosti kalcijevega sulfata
 Videz kalcijevega sulfata
Videz kalcijevega sulfata Molekularna formula
Primera4 · NH2O.
Brezvodna molekulska teža
136,134 g/mol.
Vonj
To je stranišče.
Vidik
V primeru anhidrita je videti kot beli ortorrambični ali monoklinski trden prah. Kristali so spremenljive barve: lahko so beli ali z modrikasto, sivkasto ali rdečkasto barvilo; Lahko je tudi opečna rdeča.
Gostota
2.96 GR/cm3 (brezvodna oblika). 2.32 GR/cm3 (oblika dihidrata).
Tališče
1450 ° C (2840 ° F). Značilno za močne elektrostatične interakcije med dvovalentnimi ioni ca2+ In tako42-.
Topnost
0,2-0,3 % v vodi pri 25 ° C. V vodi je malo topno in netopno v etanolu.
Stabilnost
Stabilen pri sobni temperaturi.
Uporaba kalcijevega sulfata
V gradbeništvu in umetnosti
Uporablja se pri izdelavi štukature za frizo stene domov in drugih konstrukcij, ki prispevajo k njegovemu polepšanju. Poleg tega se na strehah in okvirjih Windows izdelujejo medijski kalupi. Omet je tudi v hitri nebu.
Kalcijev sulfat se uporablja za reševanje problema, ki se pojavi pri hidraciji betona in tako sodeluje pri gradnji cest, avenij itd.
Lahko vam služi: elektrofil: reakcije, primeri, elektrofičnostZ ometom so izdelane skulpture, zlasti verske osebnosti, na pokopališčih pa se uporabljajo v nagrobnikih.
Terapevtiki
Veterinar
Eksperimentalno so bili v veterinarju uporabljeni sterilni koščki kalcijevega sulfata za popravilo kostnih napak ali votlin, kot so tiste, ki jih pustijo rane ali tumorji.
Omet ali pariški omet se lahko uporabi za popravljanje okvar kosti za njihovo edinstveno sposobnost spodbujanja osteogeneze. X -ray in Technecium študije (TC99M) Medronat.
Regeneracija kosti je bila dokazana pri šestih psih v obdobju od 4 do 6 mesecev. Kalcijev sulfat se je na tem področju začel uporabljati leta 1957 v obliki pariških tablet, ki so lahko zapolnile pasje kosti.
Nadomeščanje kosti kalcijevega sulfata je primerljivo s tistim, ki ga opazimo v avtogeni kosti.
Ruhaimi (2001) je uporabil kalcijev sulfat v novo uničeni zajčji čeljustni kosti, pri čemer je opazoval povečanje osteogeneze in kalcifikacije kosti.
Zdravilo
Kalcijev sulfat se v medicini uporablja za imobilizacijo sklepov, ki so utrpeli dislokacije in v zlomljenih kosteh, poleg tega, da se pri izdelavi tablet uporablja kot pomočnica.
Odontologija
V zobozdravstvu se uporablja kot osnova za izdelavo zobnih protez, v restavracijah in vtisih zob.
V izdelavi hrane
Uporablja se kot koagulant pri izdelavi tofuja, hrane, narejene s sojo in velike porabe v vzhodnih državah kot nadomestek mesa. Poleg tega se uporablja kot ponovno potrditev hrane in pri zdravljenju moke.
Vam lahko služi: alotropijaKot gnojila in balzam pridelkov tal
Omet (primer4· 2H2O) V Evropi so ga uporabljali kot gnojilo od 18 let.
Kalcij mora biti na voljo za korenine rastlin za ustrezno oskrbo. Nato dodajanje kalcija izboljša vrtnarske in arašidove pridelke (arašidi).
Gniloba arašidovih korenin, ki jih proizvajajo biološki patogeni, pa tudi apikalna gniloba lubenice in paradižnika, je delno nadzorovana z uporabo kmetijskih ometov.
Omet pomaga zmanjšati disperzijo gline, kar povzroči nastanek krast na tleh. Z zmanjšanjem krast, ki nastanejo na tleh, omet olajša izhod sadik. Prav tako poveča vstop zraka in vode na tla.
Omet pomaga izboljšati tla z ublažitvijo kislosti in toksičnosti aluminija, s čimer prilagaja pridelek za natrijeva tla.
V proizvodnji drugih spojin
Kalcijev sulfat reagira z amonijevim bikarbonatom, da tvori amonijev sulfat. Uporablja se tudi v procesu proizvodnje žveplove kisline.
Ashidro kalcijev sulfat mešamo s skrilavcem ali vitkostjo in, ko se mešanica segreje, sprosti žveplovi trioksid. Žveplov oksid je predhodnik žveplove kisline.