Kemične rešitve
- 3137
- 824
- Dexter Koch
Pojasnjujemo, katere kemične rešitve, njihove značilnosti, vrste, ki obstajajo, in dajejo več primerov
 Kemikalija je homogena mešanica med dvema snovma
Kemikalija je homogena mešanica med dvema snovma Kaj so kemične rešitve?
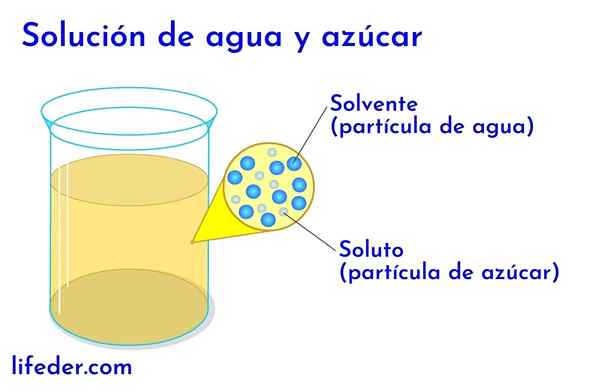
The Kemične rešitve So homogene mešanice med topilom in eno ali več topilo. Najpreprostejše rešitve tvorijo eno samo topilo in topilo, na primer, ko raztopimo sladkor v vodi, vendar obstajajo rešitve, ki lahko postanejo zelo zapletene s stotimi topili.
Najpogostejše rešitve so v tekočem stanju in v večini primerov je topilo voda. Zaradi tega se voda običajno imenuje "Univerzalno topilo". Toda rešitve niso omejene na tekočine, saj obstajajo rešitve v plinasti in trdnem stanju.
Topilo lahko najdete tudi v različnih stanjih. Na primer, tekoče raztopine s trdnimi topili (na primer sol), tekočine (na primer alkohol) ali plinaste (na primer ogljikov plin v brezalkoholnih pijačah) je mogoče imeti trdne raztopine).
Kako prepoznati topilo in topilo?
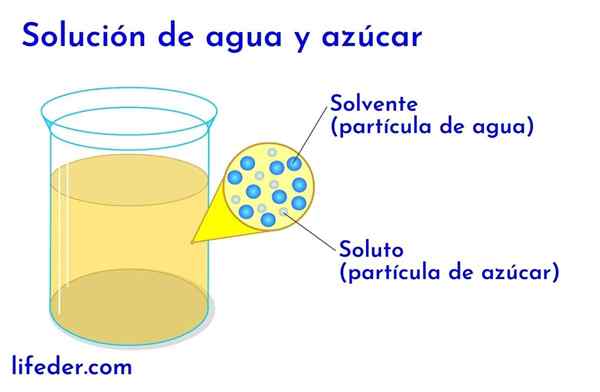 Topilo in topilo v vodi s sladkorjem
Topilo in topilo v vodi s sladkorjem V kateri koli raztopini, v kateri je voda, velja za topilo. V vseh drugih primerih topilo ustreza komponenti, ki je v večji količini ali v večjem deležu in je skoraj vedno tekočina. Druge komponente, ki so prisotne v rešitvi.
Poglejmo dva primera:
- V raztopini vode in sladkorja je voda topilo in sladkor.
- Izopropilni alkohol, ki ga kupujemo v lekarni, je rešitev, ki jo tvori voda in alkohol. V tej raztopini je topilo vode, čeprav je v manjšem deležu kot alkohol.
Značilnosti in lastnosti kemijskih rešitev
So homogene mešanice
Raztopine so mešanice, pri katerih topila topila ni mogoče razlikovati bodisi z golo oko, bodisi z uporabo povečevalnega stekla ali mikroskopa.
Imajo enotno sestavo
To pomeni, da bo kateri koli del rešitve vedno imel enake komponente (topilo in topilo) do enake koncentracije.
Vam lahko služi: kadmij (cd): zgodovina, lastnosti, struktura, uporabeZa njih je značilna njihova koncentracija
Koncentracija je ena najpomembnejših značilnosti rešitve, saj določa veliko njegovih lastnosti.
So prosojni (prozorni)
Tekoče raztopine morajo biti prosojne, to je, da jih mora svetloba imeti možnost, da jih prečkajo brez razprševanja.
So stabilni
Rešitev, v kateri topilo in topilo ne reagirata drug na drugega, bo stabilna v nedogled. To pomeni, da se sčasoma ne bo spremenil, če bo njegova sestava ostala konstantna (topilo na primer ne izhlapi).
Njegove fizikalne in kemijske lastnosti so drugačne od lastnosti topila
Fizikalne in kemijske lastnosti topila se spremenijo pri mešanju s topilom. Na primer, rešitve imajo večjo vrelišče, spodnjo tališče in imajo tudi visok osmotski tlak v primerjavi s čistim topilom.
Lahko jih ločimo skozi nekaj fizikalnih in kemičnih procesov
Rešij ni mogoče ločiti s filtracijo, centrifugiranjem ali dekantiranjem. Med drugim jih lahko ločimo le s fizikalnimi ali kemičnimi metodami, kot so kristalizacija, destilacija, izhlapevanje, reverzna osmoza in kromatografija.
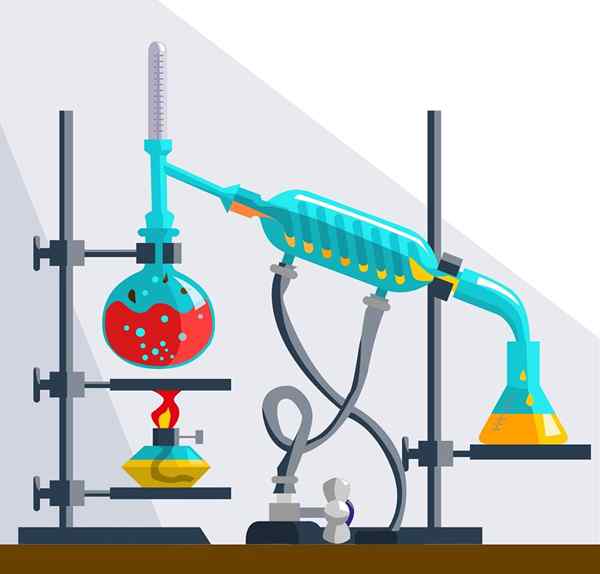 Instrumenti za destilacijo
Instrumenti za destilacijo Vrste kemijskih rešitev
Kemične rešitve je mogoče razvrstiti glede na njihovo koncentracijo glede na njihovo fizično stanje in glede na naravo topila:
Glede na vašo koncentracijo
- Nenasičene rešitve: To so tisti, v katerih topilo še ni dosegel največje koncentracije v topilu. Zaradi tega lahko več topljene raztopimo za pripravo bolj koncentrirane raztopine.
- Nasičene rešitve: To so rešitve, v katerih topilo ne more več raztopiti več topljenca. V teh primerih je vedno del topljene, ne da bi se raztopilo. Na primer, če dodamo veliko soli v kozarec z vodo, se del te soli ne bo raztopil in ostal na dnu kozarca.
- Superadirane rešitve: To so rešitve, v katerih je več raztopljenega topljenega, kot priznava topilo. To je mogoče doseči s segrevanjem nasičene raztopine, da se raztopi še več topljene, nato pa se počasi ohladi do začetne temperature. Te raztopine so nestabilne, saj lahko vsaka motnja, kot so vibracija ali majhen delček prahu na površini.
Glede na vaše fizično stanje
- Tekoče rešitve: Najpogostejši so. V tej vrsti raztopin je topilo tekočina (na primer voda, alkohol, olje itd.), Vendar je topilo mogoče najti v katerem koli stanju (trdna, tekočina ali plin). Nekaj primerov tekočih raztopin so slana voda, vino in brezalkoholne pijače.
- Trdne rešitve: V teh primerih sta tako topilo kot topilo v trdnem stanju. Najpogostejši primeri te vrste rešitev so kovinske zlitine, kot so bron, jeklo in medenina, obstajajo pa tudi drugi primeri, kot je steklo.
- Plinaste rešitve: Kot že ime pove, so homogene mešanice, v katerih so vse komponente v plinastih stanju.
Glede na topilo
- Vodne rešitve: Če je v raztopini topilo voda, potem je rečeno, da gre za vodno raztopino. To so najpogostejše rešitve, ki jih lahko najdemo v vsakdanjem življenju.
- Alkoholne rešitve: Najpogosteje topilo po vodi je alkohol. Med najpogostejšimi alkoholi so metanol, etanol in izopropil alkohol.
- Rešitve v drugih organskih topilih: Obstaja veliko drugih organskih spojin, ki se uporabljajo kot topila. Sem spadajo nekateri alkani, večina etrov, tekočih ketonov in drugih.
Primeri kemijskih rešitev
Limonada
Je vodna raztopina, ki jo tvori voda kot topilo in limonin sok ter sladkor kot topilo.
Morska voda
Morska voda ali slana voda je vodna raztopina, sestavljena iz vode in mešanice soli. Med temi soli je najbolj delež natrijevega klorida (NACL), znanega kot običajna mizna sol.
Vam lahko služi: živosrebrni oksid (HG2O)Koncentriran sirup
To je vodna raztopina, skoraj nasičena s sladkorno vodo.
Gazirana voda
Karzirana voda, znana tudi kot soda, je vodna raztopina plinastega ogljikovega dioksida (CO2) V vodi.
Zrak
Zrak je plinasta raztopina, v kateri lahko dušik obravnavamo kot topilo in kisik ter druge pline kot topilo.
Pojasnjeno maslo
Z taljenjem masla in odstranitvijo vso peno dobimo prozorno rumeno raztopino, imenovano razjasnjeno maslo. To je rešitev, v kateri sta tako topilo kot topila debela.
Barvno steklo
Barvno steklo so raztopine iz trdnega stanja, v katerih je topilo staljeni silicijev dioksid, topilo.
Kava
To je zapletena vodna raztopina, ki vsebuje veliko topljencev (med njimi kofein), ki dajejo pijači njeno značilno aromo in okus.
Jeklo
Jeklo je zlitina ali trdna raztopina, ki jo tvori kovinsko železo in grafitni ogljik.
Krvna plazma
Krvna plazma je raztopina, ki jo dobimo po centrifugiranju krvi, da odstranimo vse celice in druge suspendirane trdne snovi. To je dokaj koncentrirana vodna raztopina, ki vsebuje na stotine topljencev, vključno z ogljikovimi hidrati, aminokislinami, topnimi beljakovinami in elektroliti.
Reference
- Chang, R. in Goldsby, k. (2014). Kemija. 11. izd. New York: McGraw-Hill Education.
- Rešitev (25. januarja 2021). V Wikipediji.org.
- Rjava, t. L., Lemay, e. (2018). Kemija: osrednja znanost. 14. izdaja. Pearson.
- Krestonosich, s., in drugi. (1992). Rešitve. Uredništvo Miró.
- Vidal, J. Do. (Urednik) (1997). Interaktivni mentor - študentska tematska enciklopedija. Uredništvo oceana. Barcelona.

