Atomski radio
- 5046
- 114
- Mr. Shane Larkin
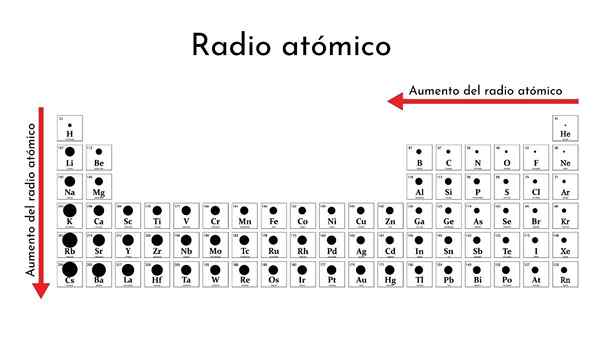
 Periodična tabela elementov z atomskimi radijskimi sprejemniki
Periodična tabela elementov z atomskimi radijskimi sprejemniki Kaj je atomski radio?
On Atomski radio Je pomemben parameter za periodične lastnosti elementov periodične tabele. Neposredno je povezan z velikostjo atomov, saj so večji radio, večji ali zajetni. Prav tako je povezan z elektronskimi značilnostmi istega.
Medtem ko ima atom več elektronov, večja je njegova atomska velikost in radio. Oba sta opredeljena z elektroni plasti Valencije, ker se na razdaljah zunaj njihovih orbite verjetnosti, da bi našli elektron, približuje nič. V bližini jedra se pojavi nasprotno: verjetnost iskanja elektrona se poveča.
 Paket bombažne kroglice. Način, kako so stisnjeni
Paket bombažne kroglice. Način, kako so stisnjeni Zgornja slika predstavlja embalažo bombažne kroglice. Upoštevajte, da je vsaka obdana s šestimi sosedi, ne da bi štela drugo možno ali spodnjo vrstico. Način stiskanja bombažnih kroglic bo opredelil njihove velikosti in s tem tudi njihove radie; Kot pri atomih.
Elementi v skladu s kemično naravo tako ali drugače sodelujejo z lastnimi atomi. Zato se velikost atomskega polmera razlikuje glede na vrsto prisotne vezi in s trdno embalažo njegovih atomov.
Kako se meri atomski polmer?
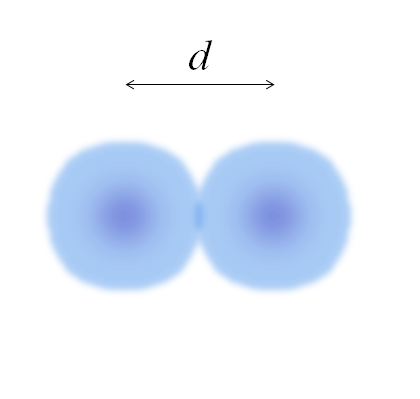 Slika dveh atomov, katerih robovi niso v celoti definirani. Vir: Gabriel Bolívar
Slika dveh atomov, katerih robovi niso v celoti definirani. Vir: Gabriel Bolívar Na prejšnji sliki je lahko preprost. Vendar sfera atoma ni popolnoma definirana. Ker? Ker elektroni krožijo in zameglijo v betonskih območjih prostora: orbitale.
Zato lahko atom obravnavamo kot kroglo z nepremagljivimi robovi, kar je nemogoče zagotovo reči, kje se končajo. Na primer, na vrhunski sliki je območje središča, blizu jedra, izgleda bolj intenzivna barva, medtem ko so njeni robovi zamegljeni.
Vam lahko služi: solvacijaSlika predstavlja diatomsko molekulo in2 (Kot Cl2, H2, Tudi2, itd.). Ob predpostavki, da so atomi sferična telesa, če je bila določena razdalja d To ločuje obe jedri v kovalentni povezavi, potem bi bilo dovolj, da jo razdelimo na dve polovici (d/2) pridobiti atomski polmer; natančneje, kovalentni polmer e za e2.
Kaj pa, če E ni oblikoval kovalentnih vezi s seboj, vendar je bil to kovinski element? Tako d Označeno bi bilo s številom sosedov, ki obdajajo E v svoji kovinski strukturi; to je s koordinacijsko številko (n.C) atoma znotraj embalaže (ne pozabite na bombažne kroglice slike).
Določitev internuklearne razdalje
Določiti d, ki je internuklearna razdalja za dva atoma v molekuli ali embalaži, so potrebne tehnike fizične analize.
Ena najbolj uporabljenih je X -Ray Difraction. Skozi steklo seva žarek svetlobe, difrakcijski vzorec, ki je posledica interakcij med elektroni in elektromagnetno sevanje.
Odvisno od embalaže je mogoče dobiti različne difrakcijske vzorce in s tem tudi druge vrednosti d.
Če so atomi v kristalni mreži "tesni", bodo predstavili različne vrednosti d v primerjavi s tistimi, ki bi jih imeli, če bi bili "udobni".
Prav tako se lahko te internuklearne razdalje gibljejo od vrednosti, zato atomski polmer dejansko sestavlja povprečna vrednost takšnih meritev.
Kako se nanašata atomski polmer in koordinacijska številka? V. Goldschmidt je vzpostavil razmerje med obema, v katerem za n.C od 12, je relativna vrednost 1; od 0.97 za embalažo, kjer ima atom n.C, enako 8; od 0.96, za n.C, enako 6; in 0.88 za n.C od 4.
Vam lahko služi: natrijev permanganat (NAMNO4): Lastnosti, tveganjaEnote
Iz vrednosti za n.C Enako 12, veliko tabel je bilo zgrajenih, kjer se primerjajo atomski radijski sprejemniki vseh elementov periodične tabele.
Ker vsi elementi ne tvorijo takšnih kompaktnih struktur (n.C manj kot 12), v razmerju se uporablja V. Goldschmidt za izračun njihovih atomskih radijskih sprejemnikov in izražanje za isto pakiranje. Na ta način so meritve atomskih radijskih sprejemnikov standardizirane.
Toda v kakšnih enotah so izražene? Glede na d Je zelo majhne, enote Angstroma Å (10 ∙ 10-10m) ali tudi široko uporabljen, pikometer (10 ∙ 10-12m).
Kako se spremenite v periodični tabeli?
V obdobju
Atomski radijski sprejemniki, določeni za kovinske elemente, se imenujejo kovinski radijski sprejemniki, medtem ko za tiste nemetalne elemente kovalentni radijski sprejemniki (kot so fosfor, str4, ali žveplo, s8). Vendar pa je med obema vrstama radijskih sprejemnikov bolj izrazita od imena.
Od leve proti desni v istem obdobju jedro doda protone in elektrone, slednje pa so omejene na isto raven energije (glavno kvantno število).
Posledično jedro izvaja naraščajočo učinkovito jedrsko obremenitev valenčnih elektronov, ki krši atomski polmer.
Na ta način imajo nemetalni elementi v istem obdobju manjši atomski (kovalentni) radijski sprejemniki.
Spuščanje skupine
Pri spuščanju s strani skupine so omogočene nove ravni energije, ki elektronom omogočajo več prostora. Tako elektronski oblak pokriva večje razdalje, njegovo zamegljeno obrobje konča več iz jedra, zato se atomski polmer razširi.
Vam lahko služi: hidroksilna skupinaKrčenje lantanida
Elektroni notranje plasti pomagajo prisiliti učinkovito jedrsko obremenitev na valenčni elektroni. Ko imajo orbitale, ki sestavljajo notranje plasti, veliko "votlin" (vozlišč), tako kot pri orbitalih, jedro močno krči atomski polmer zaradi slabega učinka ščita.
To dejstvo je razvidno iz krčenja lantanida v obdobju 6 periodične tabele. Iz HF je precejšnjo krčenje produkta atomskega polmera orbitalov F, ki so "napolnjeni" kot blok F: Lantanoides in Actinoids se prehodi.
Podoben učinek lahko opazimo tudi z elementi bloka P iz obdobja 4. Takratni produkt šibkega zaščitnega učinka d orbital, ki jih napolnimo s potovanjem po obdobjih prehodnih kovin.
Primeri atomskih radijskih sprejemnikov
Za drugo obdobje periodične tabele so atomski radijski sprejemniki njegovih elementov:
-Li: 257 popoldne
-BE: 232 popoldne
-B: 20.00
-C: 19.00
-N: 19.00
-O: 186 popoldne
-F: 184 PM
Upoštevajte, da ima litijeva kovina največji atomski polmer (257 pm), medtem ko je fluorin, ki se nahaja na desnem koncu obdobja, najmanjši od vseh (64 PM). Atomski polmer se v istem obdobju spusti od leve proti desni in vrednosti seznama kažejo.
Litij, s tvorbo kovinskih vezi je njegov polmer kovinski; in fluorid kot oblike kovalentne vezi (F-F), njegov polmer je kovalenten.
Kaj pa, če želite izraziti atomske radijske sprejemnike v angstromskih enotah? Dovolj bo, da jih razdelite do 100: (257/100) = 2.57Å. In tako naprej s preostalimi vrednostmi.
Reference
- Kemija 301. Atomski polmeri. Okreval od: ch301.cm.Utexas.Edu
- Fundacija CK-12 (2016). Atomski polmer. Okrevano od: kem.Librettexts.org
- Trendi v atomskih polmerih. Vzet iz: uvod.Kem.Okstate.Edu
- Clackamas Community College (2002). Atomska velikost. Pridobljeno iz: dl.Clackamas.Edu
- Clark J. (2012). Atomski in ionski polmer. Okrevano od: Chemguide.co.Združeno kraljestvo
- Shiver & Atkins. (2008). Anorganska kemija (četrta izdaja, str. 23, 24, 80, 169). MC Graw Hill.

