Kaj so anorganske kemijske funkcije?
- 850
- 222
- Stuart Armstrong
The Anorganske kemijske funkcije To so tiste družine anorganskih spojin, ki imajo podobne kemijske značilnosti. Te kemijske funkcije so sestavljene iz petih skupin: oksidi, baze ali hidroksidi, kisline, soli in hidrorze.
Vsaka kemična funkcija je opredeljena z igrami atomov, ki jih identificirajo. Na ta način je mogoče prepoznati funkcijo, ki ji pripada kemična spojina v skladu z njegovimi elementi.

V tem smislu lahko trdimo, da skupina OH definira kemijsko funkcijo hidroksida. Zato bo NAOH (natrijev hidroksid) pripadal skupini hidroksida.
Anorganske kemijske funkcije so vredne uporabe kemičnih spojin mineralnega izvora. Sol, voda, zlato, svinec, omet in talk, je nekaj primerov anorganskih spojin za vsakodnevno uporabo.
Vse anorganske spojine obstajajo na planetu Zemlja, preden je življenje nastalo. Z atomsko teorijo, razvojem periodične in radijske mize je bilo mogoče določiti pet funkcij anorganske kemije.
Prve preiskave in pristopi na to temo so potekale na začetku 19. stoletja in so temeljile na preučevanju preprostih anorganskih spojin (soli in plinov).
[TOC]
Anorganske kemijske funkcije
- Oksidi
 Rdeča svinec, kristalna spojina, ki vsebuje svinčev oksid. Vir: BXXXD [GFDL (http: // www.GNU.Org/copyleft/fdl.html) ali cc-be-sa-3.0 (http: // creativeCommons.Org/licence/by-sa/3.0/)], prek Wikimedia Commons
Rdeča svinec, kristalna spojina, ki vsebuje svinčev oksid. Vir: BXXXD [GFDL (http: // www.GNU.Org/copyleft/fdl.html) ali cc-be-sa-3.0 (http: // creativeCommons.Org/licence/by-sa/3.0/)], prek Wikimedia Commons Oksidi so dvojne ali binarne spojine, kjer je en ali več kisikovih atomov kombinirano z drugimi elementi. Zaradi tega obstajajo številne vrste oksidov v različnih stanjih snovi (trdna, tekočina in plinasta).
Kisik vedno zagotavlja oksidacijsko stanje -2 in skoraj vsi elementi, ki se združujejo z njim, povzročajo stabilne spojine v različnih stopnjah oksidacije.
Zahvaljujoč tem imajo pridobljene spojine različne lastnosti in imajo lahko kovalentne in ionske trdne snovi.
Osnovni oksidi
Osnovni oksidi so spojine, pridobljene iz mešanice kisika s kovino (prehod, alkalen ali alkalen). Na primer, kombinacija magnezija s kisikom povzroči osnovni oksid, kot je ta:
Vam lahko služi: elektronegativnost2mg + o2 → 2 mgO
Kovina + kisik = osnovni oksid
2mgo = osnovni oksid
Nomenklatura
Nomenklatura oksidov je vedno enaka. Najprej je navedeno generično ime spojine (oksid), nato pa je napisano ime kovine. To se zgodi, dokler je kovinska valencia pritrjena.
Primer je lahko natrijev oksid ali NA2O, kjer je najprej kovinski simbol in nato kisik s svojo valenco ali oksidacijo -2.
V primeru osnovnih oksidov obstajajo tri vrste nomenklature: tradicionalna, atomska in zaloga. Imenovanje vsakega osnovnega oksida bo odvisno od valenčne ali oksidacijske številke vsakega elementa.
Značilnosti
- Vedno se oblikujejo tako, da kombinirajo kateri koli element s kisikom.
- Binarni oksidi so tisti, ki jih dobimo z mešanjem kisika z drugim elementom.
- Za pridobitev trinalnega ali mešanega oksida je treba kombinirati binarno spojino z vodo (H2O).
- Obstajajo mešani oksidi, ki so posledica kombinacije dveh različnih elementov s kisikom.
- Baze ali hidroksidi
 Baze
Baze Njegov okus je grenka, njena tekstura je milna na dotik, dobri so prevodniki električnega toka, saj so v vodni raztopini, sodre in ko se dotikajo vijačnega papirja.
Značilnosti
- Izhajajo iz mešanice osnovnega oksida z vodo.
- Snovi, ki jih ustvarijo, lahko prejmejo protone.
- So električni vodniki, imenovani elektroliti.
- V vodi so topni, ko pridejo v stik z istim.
- Njegov okus je grenki.
- So jedke za kožo.
- Kisline
 Ocetna kislina, šibka kislina, daruje proton (vodikov ion, poudarjen v zeleni barvi) v vodo v reakciji ravnotežja, da se da acetatni ion in hidronijev ion. Rdeča: kisik. Črna: ogljik. Bela: vodik.
Ocetna kislina, šibka kislina, daruje proton (vodikov ion, poudarjen v zeleni barvi) v vodo v reakciji ravnotežja, da se da acetatni ion in hidronijev ion. Rdeča: kisik. Črna: ogljik. Bela: vodik. Kisline so anorganske spojine, ki so posledica mešanja vodika s katerim koli elementom ali skupino elementov z visoko elektronegativnostjo.
Zlahka jih je mogoče prepoznati s kislinskim okusom, saj lahko kožo zažgejo, ko stopijo v neposreden stik z njo in zaradi njihove sposobnosti, da spremenijo barvo modre v roza hrbtenico.
Vam lahko služi: dušikove valenceHidracy
Hidracidi so skupina kislin, pridobljenih iz kombinacije vodika. Primer je lahko kombinacija klora z vodikom, ki ima za posledico klorovodikovo kislino, kot je ta:
Cl2 + H2 → 2HCl
Brez kovine + vodik = hidrace
H2Cl = hidracija
Oxcacidi
Oksacidi so skupina kislin, pridobljenih iz vodne kombinacije s kislim oksidom. Primer je lahko kombinacija žveplovega trioksida z vodo, ki ima za posledico žveplovo kislino, kot je ta:
SO3 + H2O → H2SO4
Oksidna kislina + voda = oxácido
H2SO4 = Oxacid
Značilnosti
- Kožo kurijo, ker so jedke.
- Njegov okus je kisel.
- So električni tokovni vodniki.
- Ko reagirajo z osnovo, tvorijo sol in vodo.
- Ko reagirajo s kovinskim oksidom, tvorijo sol in vodo.
- Greš ven
Prodaja so spojine, ki izhajajo iz kombiniranja baze s kislino. Na splošno imajo slan okus in so v kislem stanju.
So dobri električni vodniki v vodnih raztopinah. V stiku s papirjem lakmusa ne vplivajo na njegovo barvo.
Haloides
Haloidne soli so tiste, ki nimajo kisika in se tvorijo z naslednjimi reakcijami:
1 - Pri mešanju s halogensko kovino. Primer je lahko kombinacija magnezija s klorovodikovo kislino, ki tvori magnezij in vodikov klorid, kot je ta:
Mg + 2HCl → mgcl2 + h2
2 - Pri mešanju aktivne kovine s hidrace. Primer je lahko kombinacija bromhorjeve kisline z natrijevim oksidom, kar ima za posledico natrijev in vodni bromid, kot je ta:
2HBR + 2NAO 2 → NABR + H2O
3 - Pri mešanju hidratacije s kovinskim oksidom. Primer je lahko kombinacija klorovodikove kisline z natrijevim hidroksidom, da tvori natrijev in vodni klorid, kot je ta:
Lahko vam služi: Isoamilo acetat: struktura, lastnosti, sinteza in uporabeHCl + NaOH → NACl + H2O
- Oksizala
 Natrijev bikarbonat, oksizalna
Natrijev bikarbonat, oksizalna Oksizali so tiste soli, ki vsebujejo kisik. Oblikovani so na naslednji način:
1 - Pri mešanju hidracence s hidroksidom. To je postopek nevtralizacije. Primer je lahko mešanica magnezija z žveplovo kislino, ki tvori magnezij in vodni sulfat, kot je ta:
Mg + H2SO4 → MGSO4 + H2O
2 - Pri mešanju oksacida z aktivno kovino. Primer je lahko kombinacija kalcijevega hidroksida z ogljikovim dioksidom, ki ima za posledico karbonat kalcija in vode, kot je ta:
CA (OH) 2 + CO2 → CACO3 + H2O
3 - Pri mešanju hidroksida z anhidridom.
4 - Pri mešanju hidroksida z oksacidom. Primer je lahko kombinacija dušikove kisline z barijevim hidroksidom, da bi povzročila barijev in vodni nitrat, kot je ta:
2HNO3 + BA (OH) 2 → BA (NO3) 2 + 2H2O
Značilnosti
- Imajo slan okus.
- Lahko so kisle ali osnovne.
- So dobri električni vozniki.
- Hidrorji
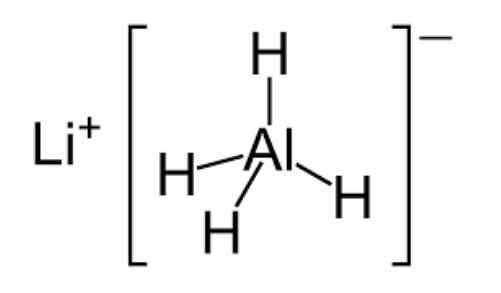
 Aluminijast litij
Aluminijast litij Hydros so anorganske kemične spojine, ki jih tvori vodik in kateri koli nemetalni element.
Običajno so v plinastem stanju in imajo podobne lastnosti kot kisline. Vendar obstajajo določeni posebni hidurki, kot je voda (H2O), ki so lahko v tekočem stanju pri sobni temperaturi.
Nomenklatura
Za oblikovanje hidrida se simbol vodika in pozneje element napisal.
Če jih poimenujemo, se doda Uro pripona in koren ne -metala, ki določa prisotnost vodika. Nekaj primerov je naslednje:
HF = vodikov fluorid
HCl = vodikov klorid
Hbr = vodik bromuro
Reference
- (21. november 2011). Dobra domača dela.com. Pridobljeno iz oksidov, kislin, hidroksidov, haloidnih soli itd.com.
- Garcia, r. In. (2007). Anorganske kemijske funkcije in njegova nomenklatura / anorganska kemična funkcija in nomenklatura je. Trillas uredništvo.
- Hiša, j. In., & House, K. Do. (2016). Opisna anorganska kemija. London: Elsevier.
- Vasquez, l. N., & Blanco, w. In. (25. april 2013). Kemija. Pridobljeno iz oksidov, hidroksidov, kislin in soli: Chemicanataliamywendyd.Blogspot.com.
- Williams, a. (1979). Teoretični pristop k anorganski kemiji. Berlin: Springer - Verlag.

