Metoda uravnoteženja algebrja (s primeri)

- 2068
- 94
- Barry Ernser
On Metoda algebrskega ravnovesja Uporablja se v kemiji za ujemanje števila atomov na obeh straneh kemične reakcije. Kemična reakcija, ki je pravilno napisana, morajo imeti formule vseh reagentov, ki sodelujejo na levi strani, in izdelkov, tudi s svojimi formulami, na desni strani.
Ko pa imate reakcijo, je število atomov v formulah reagentov enaka številu ustreznih atomov v formulah produktov ne vedno ne vedno.
 Slika 1. Metoda uravnoteženja algebrja je preprosto orodje za uravnoteženje kemijskih enačb. Vir: f. Zapata.
Slika 1. Metoda uravnoteženja algebrja je preprosto orodje za uravnoteženje kemijskih enačb. Vir: f. Zapata. Vendar je testo ohranjeno. Na primer, poglejmo naslednjo reakcijo:
KCl3 → KCL + O2
Ta enačba ima spojino, imenovano kalijev klorat, ki se razgradi s segrevanjem v kalijevem kloridu in plinskem kisiku. Ko pa natančno gledamo, opazimo, da v molekuli klorata obstajajo 3 atomi kisika, na desni pa samo ena molekula plinskega kisika z 2 atomi.
Kar se nato stori, je, da se pomnoži s številčnim koeficientom reagenta levice, tako da je število atomov vseh sodelujočih elementov enako pred in po reakciji.
Toda ... kakšna je vrednost tega koeficienta?
[TOC]
Načini za uravnoteženje enačb
V prejšnji enačbi je enostavno določiti ustrezne koeficiente s pregledom. Če se na levi pomnožimo za 2, imamo 2 atoma K, 2 Cl in 6 O.
Zato na desni pomnožimo kalijev klorid z 2 in O2 do 3:
2 kclo3 → 2KCl + 3o2
In zdaj lahko vidimo, da je računovodstvo pravilno na obeh straneh puščice in je bila reakcija uravnotežena. Upoštevajte, da lahko tudi druge numerične vrednosti povzročijo uravnoteženo enačbo, na primer:
Vam lahko služi: borna kislina: kemična struktura, lastnosti, priprava, uporabe4 kclo3 → 4KCl + 6o2
Vendar je treba vedno iskati nabor celotnih minimalnih števil, ki so enaki količini atomov na obeh straneh.
Kličejo se številke, ki pomnožijo vsako formulo koeficienti. Zelo pomembno je opozoriti, da se lahko koeficienti dodelijo za ravnotežje, vendar morajo naročniki ostati tako, kot so prikazani v vsaki formuli.
Prav tako ni mogoče vstaviti koeficientov na sredini formule vsake spojine, saj bi jo spremenili.
Preproste enačbe, kot je primer, je mogoče uravnotežiti s pregledom ali oceno. Za tiste, ki so nekoliko bolj zapleteni, obstaja algebrska metoda z nizom preprostih korakov in osnovnih aritmetičnih operacij.
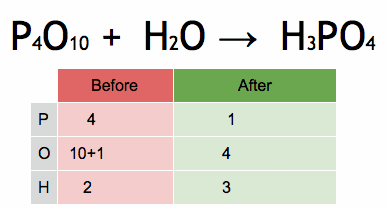 Slika 2. Animacija, ki prikazuje uravnoteženje kemične enačbe za pridobitev fosforne kisline. Vir: Wikimedia Commons. Ephert/cc by-sa (https: // creativeCommons.Org/licence/by-sa/4.0
Slika 2. Animacija, ki prikazuje uravnoteženje kemične enačbe za pridobitev fosforne kisline. Vir: Wikimedia Commons. Ephert/cc by-sa (https: // creativeCommons.Org/licence/by-sa/4.0 Koraki za algebraično uravnoteženje kemične enačbe
Korak 1
-Vsaki molekuli dodelite poljubni koeficient, ki ga simbolizira pismo. Besedila A, B, C, D .. ., Po potrebi po potrebi.
Pomembno: Spomnimo se, da molekula uporablja samo koeficient in se na sredini nikoli ne prepleta, vedno je nameščen na levo.
2. korak
-Naredite seznam vsakega sodelujočega elementa.
Korak 3
-Postavite koeficient ali koeficiente, dodeljene vsaki spojini na levo, in se ujemajte s tistimi na desni. Če obstajajo naročniki, se pomnožijo s koeficientom, da bi našli skupno število atomov.
In če se kateri koli element najde v več kot eni molekuli, se dodajo količine atomov na vsaki strani. Na ta način delne enačbe vsakega elementa.
4. korak
-Numerična vrednost je dodeljena enemu od koeficientov. Običajno je ta številčna vrednost 1 in je dodeljena črki, ki se pojavi večkrat. To doseže preprosto enačbo, ki služi kot izhodišče za iskanje drugih koeficientov.
Vam lahko služi: faktor redčenja5. korak
-Preprosto aritmetiko določite vrednost naslednjega koeficienta in nadomestite njegovo vrednost v drugi enačbi, da dvignete novo.
6. korak
-Ponovite prejšnji korak, da zamenjate vrednosti in ustvarite novo enačbo, dokler ne najdete vseh koeficientov.
7. korak
-Zamenjajte tako določene vrednosti. Če so te vrednosti celotne, je treba preveriti, ali je bila enačba uravnotežena. Če niso bile cele, se pomnoži z minimalnim skupnim večkratnim imenovalcem in ravnotežje se preveri.
Nato bomo uporabo teh korakov vizualizirali pri reševanju nekaterih primerov.
Rešeni primeri uravnoteženja
Primer 1
Po potrebi uravnotežite naslednjo reakcijo z algebrsko metodo:
N2Tudi5 → n2Tudi4 + Tudi2
Rešitev
Opažamo, da reakcija ni uravnotežena, ker čeprav obstajata 2 dušikova atoma na obeh straneh, s kisikom na levi in desni so različni.
Nato moramo slediti korakom, opisanim v prejšnjem razdelku:
-Enačbo znova napišemo in vsako molekulo pomnožimo z drugačnim koeficientom. Izbrane so male črke, tako da jih ne zmedejo z elementi:
A⋅n2Tudi5 → B⋅n2Tudi4 + C⋅O2
-Zdaj naštejemo vsak element in se znesek tega elementa ujemamo z levo in desno. To so delne enačbe za vsak element:
- A⋅n2 = B⋅n2
- A⋅O5 = B⋅O4 + C⋅O2
-Pomnožitev koeficienta in podpisov dobimo število dušikovih atomov. Iz enačbe 1 dobimo:
2a = 2b
-Enačbe 2 5 atomi kisika na levi, medtem ko so na desni strani 4b in 2 c:
5A = 4B + 2C
-Na ta način dodelimo vrednost 1 koeficientu a:
A = 1
Ta izbira je poljubna, lahko bi jo izbrali tudi najprej B = 1.
-Te vrednosti se nadomestijo v enačbi 2, da se določi vrednost C:
Lahko vam služi: cupric oksid (cuo)5 = 4 + 2c
2C = 5-4 = 1
C = ½
-Koeficiente nadomestimo v prvotni enačbi, 1 ni potrebno, da bi jih napisali izrecno:
N2Tudi5 → n2Tudi4 + ½ o2
-Ker je zaželeno, da so koeficienti celotni, se celotna enačba pomnoži z minimalnim skupnim večkratnim večkratnikom, ki sta 2 in 1:
m.c.m. (1.2) = 2
Nato se z pomnoževanjem levo in desno do 2 pridobi:
2N2Tudi5 → 2n2Tudi4 + Tudi2
In štejemo število atomov na obeh straneh, da preverimo ravnotežje:
- N levo: 4
- Ali levo: 10
- N desno: 4
- Ali desno: 8 + 2 = 10
Primer 2
Uravnotežite naslednjo kemijsko reakcijo:
Nahco3 → NA2Co3 + H2Ali + co2
Rešitev
Vsako molekulo pomnožimo z drugačnim koeficientom:
A⋅ nahco3 → B⋅na2Co3 + C⋅H2O + d⋅co2
Nato predlagamo računovodstvo vsakega elementa desno in levo od puščice. V reakciji je skupno 4 elemente: natrij NA; Vodik H; Avtomobil in kisik ali vse je treba šteti:
- A⋅na = b⋅na2
- a⋅H = C⋅H2
- A⋅c = b⋅c + d⋅c
- A⋅O3 = B⋅O3+C⋅O+d⋅O2
V skladu z vsakim ravnovesjem se dobijo naslednje enačbe:
1) a = 2B
2) a = 2c
3) A = B + D
4) a = 3b + c + 2d
Najbolj ponavljajoč koeficient je do, Zato dodelimo vrednost 1:
A = 1
Tako:
1) a = 2b ⇒ b = ½
2) a = 2c ⇒ c = ½
3) a = b + d ⇒ d = a - b = 1 - ½ = ½
Koeficiente nadomestimo v enačbi:
Nahco3 → ½. Na2Co3 + ½. H2O + ½.Co2
Na obeh straneh puščice se pomnožimo z 2, saj je edini prisotni imenovalec za odpravo deleža:
2nahco3 → NA2Co3 + H2Ali + co2
Štejemo število atomov, ki so prisotni na levi: 2 atoma Na, H in C in 6 O. Bralec lahko preveri, ali je vsak od njih tudi v enakih količinah na desni strani.
Reference
- Atkins, str. Načela kemije: poti odkritja. Pan -american Medical uredništvo. 3. izdaja.
- Briceño, j. Vodnik za kemijo USB. Okreval od: gecousb.com.pojdi.
- Chang, R. 2013. Kemija. 11VA. Izdaja. MC Graw Hill Education.
- Rešene vaje. Algebrsko uravnoteženje. Pridobljeno iz: Sutted vaje.co.
- Simoza, l. Uravnoteženje kemijskih enačb. Okreval od: Guao.org.
- « Značilnosti mrtvih stroškov, izračun, primeri
- Značilnosti Inca Architecture in izjemne konstrukcije »

