Kovine
- 781
- 18
- Ms. Pablo Lebsack
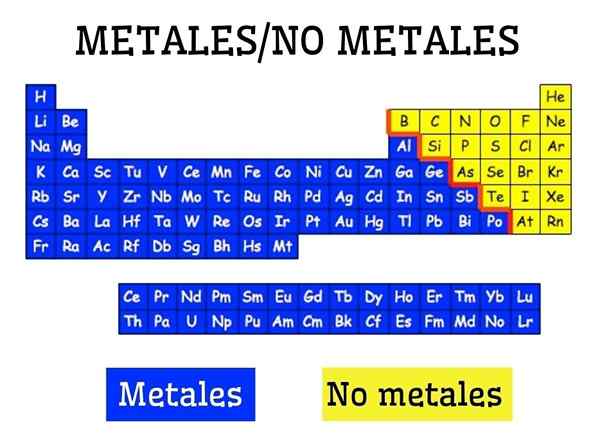
 Kovine in ne -kovine v periodični tabeli elementov
Kovine in ne -kovine v periodični tabeli elementov Kaj so kovine?
Kovine tvorijo skupina elementov, ki se nahajajo na levi strani, z izjemo nemetalnega vodika, periodične tabele. Kovine predstavljajo približno 75 % kemičnih elementov, zato je mogoče trditi, da je velik del narave kovinske.
Kovine, ki jih je človek sprva preganjal v prazgodovini, so bile naslednje: zlato, srebro, baker, kositer, svinec in železo. To je bilo posledica dejstva, da so domači ali enostavnost njihove obdelave za izvajanje komunalnih predmetov.
Zdi se, da je čarovnija veliko kamnin in mineralov, lahko izvlečemo sijoča in srebrna telesa (z določenimi pomembnimi in izjemnimi izjemami). Takšen je primer boksita in aluminija, katerih glinene kamnine ta kovina zmanjša v ploščah ali srebrnih papirjih.
Kovine so okvir industrije; Njihova ožičenje, reaktorji, enote, zabojniki, vse na tak ali drugače so sestavljene iz kovin in zlitin.
S kovinami so bili narejeni prvi kovanci, orožje, orodja, oklep in nato uporabljeni v proizvajalcih vozil, koles, ladij, letal, računalnikov, med drugimi nepogrešljivimi predmeti v sodobnem življenju.
Zgodovina
Bakrena starost
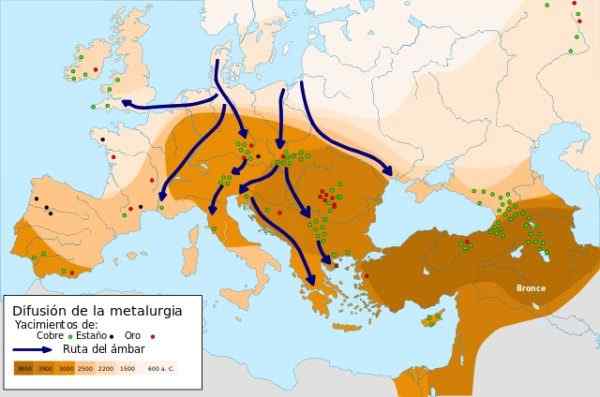 Širitev metalurgije - Vir: Metalurška difuzija.SVG v okviru Creative Commons Attribution-Compartyrigual 4 Licenca 4.0 International
Širitev metalurgije - Vir: Metalurška difuzija.SVG v okviru Creative Commons Attribution-Compartyrigual 4 Licenca 4.0 International V 9000 a.C. Prvi kovinski predmeti bakra, kovani na Bližnjem vzhodu, so bili razviti, ko je moški ugotovil, da je, ko je baker udaril. To je doba bakra.
Ugotovljeno je bilo, da lahko baker dobimo s segrevanjem modrih mineralov, kot sta Corvellita in malahit (4000-3000 do.C.).
Kallitsko obdobje je obdobje, ki je pred bronasto starostjo, kar ustreza 5000-3000.C. Moški je začel eksperimentirati z fuzijo in livarno bakra, da bi pridobil baker iz bakrenega oksida.
Bronasta doba (3000-1500 a.C.)
 Bronze Age Materials - Vir: Gaguilella pod Atribucijo Creative Commons -shareigual 4 licenca 4.0 International.
Bronze Age Materials - Vir: Gaguilella pod Atribucijo Creative Commons -shareigual 4 licenca 4.0 International. Moški je slučajno začel razviti zlitine, sprva iz bakra in arzena, nato pa z bakrom in kositrom, da bi dobil bronast na Bližnjem vzhodu.
Bronasti članki, ki ustrezajo temu času, so imeli 87 % bakra, 11 % kositra in majhne količine železa, arzena, niklja, svinca in antimona.
Železna doba (700 a.C.)
Moški je uporabil svoje izkušnje pri proizvodnji ponarejenega bakra za proizvodnjo kovanega železa na Bližnjem vzhodu. V istem časovnem obdobju je prišlo do granulacije Etruscovega prahu, Italija.
Prva znana jeklena proizvodnja, železna in ogljikova zlitina, se je pokazala v kovinskih delih na arheološkem mestu v Anatoliji (1800 do.C.)
Vam lahko služi: gravimetrija: gravimetrična analiza, metode, uporabe in primeriProti 1122 d.C., Na neznani datum in kraj se predstavi lito železo. Leta 1440 d.C. Na Kitajskem je velik zvonec v Pekingu. Skoraj tri stoletja pozneje, leta 1709 d.C., Lito železo se proizvaja z uporabo koksa kot gorljivega materiala.
Leta 1779 je bil lito železo v Angliji uporabljen kot arhitekturni material. Leta 1855 je Henry Bessenir uporabil Arrabio kot surovino za pridobivanje mehkega jekla. Angleški Clark in Wood (1872) patenta zlitina, ki se trenutno šteje za nerjaveče jeklo.
Fizikalne lastnosti kovin
 Bron teh starodavnih zvonov kaže na uporabnost kovin za okrasne ali verske namene. Vir: pxhere.
Bron teh starodavnih zvonov kaže na uporabnost kovin za okrasne ali verske namene. Vir: pxhere. Med nekaterimi fizikalnimi lastnostmi kovin imamo:
-Kovine so briljantne in lahko odražajo svetlobo.
-Na splošno so dobri prevodniki električne energije in toplote.
-Imajo visoko fuzijsko in vrelišče.
-So poševni, to je, da jih je mogoče zabiti, da proizvajajo nizke debele liste.

-So duktilni, z njimi lahko izdelujete žice ali vlakna zelo malo premera.
-Predstavljeni so v trdnem stanju, z izjemo živega srebra, da je pri sobni temperaturi v tekočem stanju, in galij, ki se topi samo z zategovanjem v rokah v rokah. Na naslednji sliki si lahko ogledate vsebnik živega srebra:

-So neprozorna telesa, njihove tanke rjuhe ne prekriža svetlobe.
-Imajo veliko trdoto, razen natrija in kalija, ki jih lahko reže nož.
-Imajo visoko gostoto, ki sta osmij in iridij najvišjega, litij z najnižjo gostoto.
Kemične lastnosti kovin
Med nekaterimi kemičnimi lastnostmi kovin imamo:
-Ponavadi izgubijo elektrone in tvorijo kovinske katione, mn+, kjer N označuje njegovo oksidacijsko številko, ki samo za alkalne in alkalistične kovine sovpada z njegovo valenčno številko.
-Njegove elektronegativnosti so nizke.
-Tečejo in doživljajo oksidacijsko škodo.
-Ob reakciji s kisikom tvorijo osnovne okside. Ti oksidi v kombinaciji z vodo tvorijo kovinski hidroksidi. Kovinski oksidi reagirajo s kislinami, da tvorijo soli in vodo.
-So dobra sredstva za zmanjšanje, saj dajo svoje elektrone.
Vrste kovin
Kovine so razvrščene kot naslednje: alkalno, alkalno-preskusno, post-tranzicijsko, prehodno in tako imenovano redko zemljo.
Alkalne kovine

Običajno se ne znajdejo svobodne, ker zlahka oksidirajo. Imajo suborbital s1 V svoji zunanji orbitalni plasti, zato imajo stanje oksidacije +1. So kovine, ki eksotermično reagirajo z vodo in se močno zmanjšujejo.
Kovine alkalne-Térreos
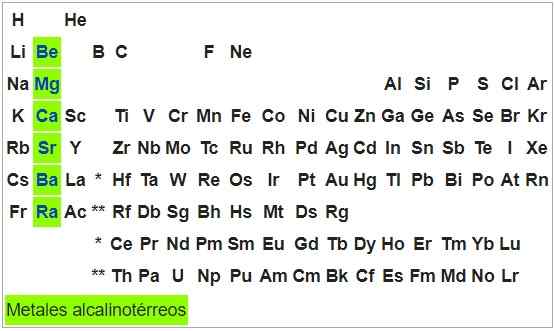
So popravljive in duktilne kovine. Atomi elementov te skupine imajo konfiguracijo S2, Tako lahko dajo dva elektrona in njihov status oksidacije je +2. Z izjemo berilija so oksidacijski za izpostavljenost zraku.
Vam lahko služi: ogljikovi alotropiPosttransionalne kovine
So kovine tako imenovanega bloka P, ki se nahaja med prehodnimi kovinami in metaloidi v periodični tabeli.
Elementi skupine 3 imajo kot najpogostejša oksidacijska stanja +1 in +3, čeprav aluminij predstavlja samo stanje oksidacije +3. Je tudi del post -tranzicijskih kovin, ki se nahajajo v skupinah 14 in 15.
Prehodne kovine d
Tvorijo skupino med osnovnimi elementi in kislinskimi -formatorji. Atomske orbitale D in F sta nepopolna in se napolnita. Čeprav se izraz prehodne kovine nanaša na prehodne kovine D.
Prehodne kovine imajo več kot eno oksidacijsko stanje. Imajo fuzijsko in vrelišče višje od drugih kovinskih skupin. Prehodne kovine je zelo heterogena kovinska skupina, ki med drugim vključuje železo, krom, srebro itd.
Redka zemlja
 Redki mineral Zemlje
Redki mineral Zemlje To skupino kovin sestavljajo elementi Scandio in Ititrio ter elemente serije lantanidov in aktinidov. Izraz "redka zemlja" se nanaša na dejstvo, da jih v naravi ne najdemo v čistih stanjih in jih je pritrdimo s kislinami.
Uporaba/aplikacije kovin
Alkalne kovine
Litij se uporablja kot sredstvo za prenos toplote v nekaterih jedrskih reaktorjih. Uporablja se v nekaterih suhih baterijah in akumulatorjih malo teže. Klorid in litijev bromid sta higroskopski spojini, ki se uporabljajo v procesih industrijskega sušenja in klimatske naprave.
Natrij se uporablja v kovinski metalurgiji, kot sta titanij in cirkonij. Uporablja se pri javni razsvetljavi v svetilkah natrijevega loka. Natrijev klorid (NACL) se uporablja kot okus hrane in ohranjanje mesa.
Alkalineterne kovine
Magnezij je bil uporabljen v fotografiji kot bliskavico in ognjemet. Barium je sestavni del zlitin, ki se uporabljajo v svečk zaradi enostavnosti elementa za oddajanje elektronov. Barijeve soli se uporabljajo za omejitev škode, ki jo povzročajo x -roji v ploščah prebavil.
Kalcij se uporablja za odpravo nečistoč, raztopljenih v staljenih kovinah in pri izločanju preostalih plinov v vakuumskih ceveh. Je del omet, material, ki se uporablja pri gradnji in pri zdravljenju zlomov kosti.
Posttransionalne kovine
Aluminij, ker je lahka kovina, se uporablja pri konstrukciji letal in posod. Uporablja se tudi pri izdelavi številnih kuhinjskih pripomočkov. Uporablja se kot surovina pri proizvodnji deodorantov, ki omejujejo znojenje.
Vam lahko služi: odstotne rešitveGallium se uporablja v tranzistorjih in termometrih za visoke temperature. Izotop 67GA se uporablja v medicini pri zdravljenju nekaterih melanomov. Svinca se uporablja pri gradnji baterij in za zaščito pred ionizirajočim sevanjem.
Prehodne kovine
Baker se uporablja v cevi za oskrbo z vodo, v hladilnikih in klimatskih sistemih. Uporablja se tudi kot del računalniškega mehanizma za odvajanje toplote. Uporablja se pri prevodnosti električnega toka, v elektromagnetih in v barvanju stekla.
Nikelj se uporablja pri izdelavi nerjavečega jekla, pa tudi kitarskih strun in polnilnih baterij. Uporablja se tudi v galvanoplastiki pri zaščiti kovin. Uporablja se v zlitinah, ki jih najdemo v delih vozil, kot so ventili, ležaji in zavore.
Nikelj se že dolgo uporablja v izdelavi kovancev.
Cink se uporablja pri zaščiti korozijske kovine, pri proizvodnji medenine. Cinkov oksid in cinkov sulfat se uporabljata pri izdelavi plošč, ki se uporabljajo na strehah, žlebovih in padcih.
Krom se uporablja pri zaščitni koroziji in za oskrbo sijaj. Uporablja se kot katalizator v reakciji sinteze amoniaka (NH3). Kromijev oksid se uporablja pri zaščito lesa.
Redka zemlja
Scandio se uporablja v aluminijevem aluminiju za vesoljske komponente. To je dodatek v svetilnih svetilkah.
Lantano se uporablja v visokem loma in alkaliji -odmevnem steklu. Poleg tega se uporablja pri proizvodnji kamer leč in kot katalitični katalizator za rafinerije olja.
Cerio se uporablja kot kemično sredstvo. Poleg tega se uporablja za oskrbo rumenega stekla in keramične obarvanosti, pa tudi katalizator za samozaposlene peči.
Primeri kovinskih elementov
Alkalna
Natrij (NA), kalij (K), Cezija (CS), litij (Li) in rubidij (RU).
Alkalno-Terreos
Berlij (BE), magnezij (mg), kalcij (CA), stroncija (MR), barij (BA) in radio (RA).
Postranzicijski
Aluminij (AL), Gallium (GA), Indian (IN), Talio (TL), kositer (SN) in svinec (PB).
Prehodni
Titanium (Ti), vanadij (v), Chrome (CR), mangan (Mn), železo (vera), kobalt (co), nikelj (ni), baker (cuinc), cink (Zn), cirkonij (Zr), Niobio (NB), Molybden (MO), Paladio (PD), Silver (AG), Volframium (W), Renio (Re), Osmio (OS), Iridido (IR),
Platinum (PT), zlato (AU) in živo srebro (HG).
Redka zemlja
Scandio (SC), Itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodymium (ND), Samarium (SM), Europ (EU), Gadolinio (GD), Holmio (HO) Erbio (ER), Tulio (TM), Iterbio (YB) in Luthacio (Lu).
Reference
- Whitten, Davis, Peck & Stanley. (2008). Kemija. (8. izd.). Cengage učenje.
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Čelada, Anne Marie, ph.D. (5. oktober 2019). Kovine v primerjavi z nemetali. Okreval od: Thoughtco.com
- Kovine in njihove lastnosti-fizične in kemične. [PDF]. Okreval od: csun.Edu
- Jonathan mojster. (2019). 18 različnih vrst kovine (dejstva in uporabe). Okrevano od: makeitFrommetal.com

