Hidrofilna uporaba izraza, značilnosti, primeri

- 1054
- 9
- Barry Ernser
A hidrofilni ali hidrofilni To je molekularni segment ali spojina, za katero je značilna močna afiniteta do vodnih in polarnih topil. Etimološko pomeni "ljubitelji vode", kar pomeni, da se bo hidrofilni lahko učinkovito raztopil ali učinkovito interakcijo z molekulami vode.
Zato so hidrofilne snovi ponavadi topne ali mešljive z vodo. Vendar pa hidrofilnost, torej njena afiniteta do vode in drugega polarnega topila.
 Steklo je hidrofilni material, ker se zlahka zmoči in kapljice, ki se odlagajo na njem. Vir: Pexels.
Steklo je hidrofilni material, ker se zlahka zmoči in kapljice, ki se odlagajo na njem. Vir: Pexels. Tako je hidrofilne površine lažje navlažiti ali navlažiti kot hidrofobne, tiste, ki sovražijo vodo ali jo odbijajo. Prva laskava voda pade v vrstice, medtem ko jih slednja obrne na okrog in vidne. Vizualizacija teh kapljic je eden glavnih dejavnikov za razlikovanje hidrofilnega materiala od hidrofobnega.
Koncept hidrofilnosti je ključnega pomena za razumevanje površinske kemije, rešitev, vmesnikov in amfifiličnega značaja snovi, kot so beljakovine in maščobne kisline.
[TOC]
Uporaba hidrofilnega ali hidrofilnega izraza
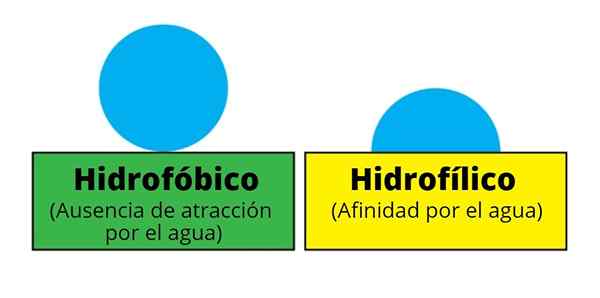
"Hidrofilni" in "hidrofilni" sta označena tako molekule kot strukturni deli istih. Vendar se „hidrofilni“ uporablja predvsem za navajanje katere koli molekule ali spojine, ki ima veliko afinitete do vode.
Zato obstaja hidrofilna ali hidrofilna molekula, če je njegova afiniteta do vode zelo visoka glede na določene premisleke. Na primer, saharoza je hidrofilna spojina, ki je isto kot pravi, da je hidrofilna, saj se njeni kristali zlahka raztopijo v kateri koli volumen vode.
Vam lahko služi: TritioZadevna molekula lahko predstavlja hidrofilne segmente ali dele, ki jih lahko sestavljajo gazirano okostje ali preprosto polarna skupina. Ko gre za skupino, ponavadi rečemo, da gre za hidrofilno skupino, ki prispeva k hidrofilnosti molekule ali površini, ki ji pripada.
Običajno se „hidrofilni“ uporablja pogosteje kot „hidrofilni“, saj si slednji običajno pridržuje več kot karkoli za molekule ali spojine, ki so popolnoma hidrofilne; to pomeni, da v svojih molekularnih strukturah nimajo hidrofobnih regij. To še posebej velja, kadar so opisane makromolekule ali polimerne trdne snovi.
Značilnosti hidrofilnih snovi
Kovalenca
Hidrofilne snovi so kovalentne spojine, kar pomeni, da njihove enote sestavljajo molekule in ne iz ionskih omrežij. Čeprav so soli ponavadi zelo topne v vodi, celo več kot mnogi hidrofilni.
Po drugi strani pa niso vse soli topne v vodi, kot je srebrni klorid, AGCL, zato jih ni mogoče uvrstiti med hidrofilne.
Polarnost
Da bi bila molekula hidrofilna, mora imeti nekaj polarnosti. To je mogoče le, če imajo polarne skupine, kot so -oh, -sh, -nh v svoji strukturi2, -COOH itd., tako da prispevajo k njihovemu trajnemu dipolnemu trenutku in s tem k njihovi hidrofilnosti.
Interakcije
Hidrofili so prepoznani nad drugimi spojinami zaradi svoje sposobnosti oblikovanja vodikovih mostov z molekulami vode. Upoštevajte, da zgoraj omenjene polarne skupine lahko donirajo vodike ali jih sprejmejo, da tvorijo takšne mostove, ki so posebna vrsta interakcij dipol-dipolo.
Trdna stanja
Hidrofili so lahko plinaste, tekoče ali trdne snovi, najpogostejša sta ta zadnji dve.
Vam lahko služi: diferencialni elektronHidrofilne tekočine se mešajo z vodo, zato ko se meša, dve fazi ne bomo videli.
Medtem se hidrofilne trdne snovi raztopijo v vodi ali jih zelo enostavno absorbirajo; Poleg tega se nekateri lahko zmočijo ali se zmočijo, ne da bi se raztopili, saj čeprav je njegova površina hidrofilna, ni povsem njegova notranja masa. To je primer številnih polimernih materialov, kot so kemično spremenjeni silikoni.
Hidrofilne površine
Hidrofilne površine so podvržene površinskim kemijskim študijam. Niso topni v vodi, lahko pa navlažijo in sploščijo kapljice vode, ki se odlagajo na njej. To je zato, ker imajo zunanje hidrofilne skupine, ki učinkovito delujejo z molekulami vode.
Kapljica vode se oblikuje s hidrofilno površino kot kontaktni kot manj kot 90 °, kar je enako, kar je mogoče reči, da bo predstavljala sploščeno, malo sferično ali okroglo obliko.
Takšno je tako, da se spustijo, da se širijo in tečejo kot tekoče vrstice. Na primer, ta lastnost se uporablja za preprečevanje megle, ki tarnate površino, saj se ga komaj dotakne vodna kondenza in zdrsne navzdol.
Naša koža je hidrofilna, saj na njej kapljice ponavadi sploščijo in zdrsnejo; Razen kadar je embriardunate olja ali smetane. Potem bodo kapljice vode okrogle in definirane, ker je površina začasno postala hidrofobna.
Primeri hidrofilnih snovi
Amoniak
Amoniak, NH3, Je hidrofilna, ker lahko njegova molekula tvori več vodikovih mostov z vodo. Zaradi tega v plinasti in tekočem stanju zelo topno v vodi.
Oksalna kislina
Oksalna kislina, h2C2Tudi4, Je hidrofil.
Vam lahko služi: Petrije: značilnosti, funkcije, uporabite primereMetanol
Metanol, ch3Oh, to je hidrofilna zahvaljujoč svoji skupini Oh.
Alkoholi
Alkoholi so običajno hidrofilne snovi, dokler njihov ogljični okostje ni zelo veliko. Na primer, 1-propanol in 2-propanol sta mešana z vodo, vendar se to ne zgodi z 1-butanolom, katerega mešljivost postane nižja zaradi svoje ogljikove verige večje dolžine.
Škrob
Škrob je primer hidrofilnega polimera, saj imajo njene glukozne enote več skupin OH, s katerimi se tvori vodni mostovi z molekulami vode.
Les
Les je hidrofilni in čeprav se ne raztopi v vodi, se hitro navlaži, če ga ne obdelamo s hidrofobnimi prevlekami.
Beljakovine
Beljakovine imajo polarne skupine zelo povezane z vodo. Zato so njegove interakcije z molekulami vode učinkovite. To pa ne pomeni, da so vsi beljakovini topni v vodi, saj imajo njihove strukture (terciarne in kvartarna) temeljno vlogo v omenjenem procesu raztapljanja.
Kozarec
Steklo je hidrofilni material, ker, čeprav ni sestavljen iz molekul, ampak SIO omrežja2 Tri -dimenzionalni, njihovi atomi kisika lahko sprejmejo mostove vodika v vodi. To je razlog, zakaj se steklena posoda znojijo v vlažnih okoljih.
Reference
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. (10th Izdaja.). Wiley Plus.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Morrison in Boyd. (1987). Organska kemija. (Peta izdaja). Addison-Wesley Iberoamericana.
- Wikipedija. (2020). Hidrofil. Pridobljeno iz: v.Wikipedija.org
- David l. Chandler. (16. julij 2013). Pojasnjeno: hidrofobni in hidrofilni. Obnovi se od: novice.MIT.Edu
- Gele. (2020). Hidrofilni materiali. Okrevano od: gelest.com
- Ahmad Darem et al. (5. september 2018). Hidrofilni in hidrofobni materiali in aplikacije. Taylor & Francis Online. doi.org/10.1080/15567036.2018.1511642

