Značilnosti glukoze oksidaze, struktura, funkcije
- 3793
- 1191
- Mr. Shane Larkin
The glukoza oksidaze, Znan tudi kot β-D-glikoza: kisik-1-oksidoraduktaza, glukoza-1-oksidaza ali preprosto oksidaza glukoza, je encim oksidorereduktaze, ki je zadolžen za oksidacijo β-D-glikoze, ki proizvaja D-glukonolakn in vodikov peroksid.
Odkrili so ga konec dvajsetih let prejšnjega stoletja v izvlečkih gliv Aspergillus niger. Njegova prisotnost je bila dokazana v glivah in žuželkah, kjer ima trajna proizvodnja vodikovega peroksida s svojim katalitičnim delovanjem pomembne funkcije v obrambi pred patogenimi glivami in bakterijami.
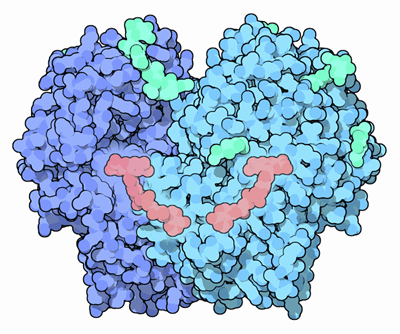
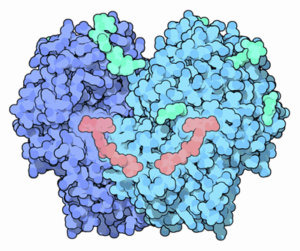 Shema strukture encima glukoze oksidaze (izvorni arkadijski, prek Wikimedia Commons)
Shema strukture encima glukoze oksidaze (izvorni arkadijski, prek Wikimedia Commons) Trenutno je bila glukoza oksidaze očiščena iz različnih glivičnih virov, zlasti iz žanrov Aspergillus in Penicillium. Čeprav lahko uporablja druge podlage, je precej selektiven za oksidacijo β-D-glikoze.
Ima več dobičkov v industrijskih in komercialnih okoliščinah, kar je posledica nizkih stroškov proizvodnje in velike stabilnosti.
V tem smislu se ta encim uporablja tako v industriji proizvodnje hrane kot v kozmetologiji, pri farmacevtu in klinični diagnozi, ne le kot aditiv, ampak kot biosenzor in/ali analitični reagent različnih raztopin in telesnih tekočin.
[TOC]
Značilnosti
Glukoza oksidaze je globularni flavoprotein, ki uporablja molekularni kisik kot sprejemnik elektronov za proizvodnjo glukoze, D-glicona-Δ-laktona in vodikovega peroksida.
V celičnem sistemu lahko proizvedeni vodikov peroksid porabi encim Catlase za proizvodnjo kisika in vode. V nekaterih organizmih se D-glukonolakton hidrolizira v glukonsko kislino, ki lahko izvaja različne funkcije.
Doslej opisani encimi glukoze oksidaze so sposobni oksidirati monosaharide in druge vrste spojin, vendar so, kot je bilo že prej, precej specifične za β D-glikozni anomer.
Lahko vam služi: razmaza krvi: značilnosti, vrste, tehnike in histologijaDelujejo v kislih pH območjih, od 3.5 do 6.5 in, odvisno od mikroorganizma, se lahko ta razpon precej razlikuje. Poleg tega je glukoza glivične oksidaze ena od treh vrst beljakovin, ki so pritrjene na ortofosfate.
Tako kot drugi biološki katalizatorji lahko tudi te encime zavirajo različne molekule, vključno s srebrom, bakrom in živo srebrom, hidrazinom in hidroksilaminom, fenilhidrazinom, natrijevim bisulfatom, med drugim.
Struktura
Glukoza oksidaze je dimični protein z dvema enakima monomerama po 80 kDa, ki ga kodirata isti gen, kovalentno združeni z dvema disulfurnima mostoma in katerih dinamičnost je vključena v katalitični mehanizem encima.
Odvisno od telesa, povprečna molekulska masa homodimera.
Monomerna struktura
Analiza monomerov različnih glukoze oksidaze, ki jo najdemo v naravi.
Domeno FAD Unije sestavljajo β-nameščeni listi, medtem ko je glukozni stičišče.
Glikozilacija
Prve študije, izvedene iz encima Do. Niger Ugotavljajo, da ima ta protein 20% sveže teže, sestavljene iz aminoazúces in da še 16-19% ustreza ogljikovim hidratom, od tega več kot 80% ročno povezanih odpadkov z beljakovinami s povezavami s povezavami s povezavami N- ali Tudi-glikozidni.
Čeprav ti ogljikovi hidrati niso bistveni za katalizo, obstajajo poročila, ki kažejo, da izločanje ali odstranjevanje teh sladkih odpadkov zmanjšuje strukturno stabilnost beljakovin. To je lahko posledica topnosti in odpornosti proti proteazam, ki mu jo daje ta ogljikovih hidratnih plasti.
Vam lahko služi: živali z vretenčarjiFunkcije
V glivah in žuželkah, kot je razpravljano, oksidazna glukoza izpolnjuje bistveno funkcijo obrambe pred patogenimi glivami in bakterijami z ohranjanjem konstantnega vira oksidativnega stresa s trajno proizvodnjo vodikovega peroksida.
Govoriti o drugih splošnih funkcijah encima glukoze oksidaze ni tako preprosto, saj ima v različnih organizmih zelo poseben dobiček, ki ga izražajo. Na primer pri čebelah njegovo izločanje iz hipofaringealnih žlez do sline prispeva k ohranjanju medu.
V drugih žuželkah, odvisno od stadiona življenjskega cikla, deluje v dezinfekciji zaustavljene hrane in pri zatiranju rastlinskih obrambnih sistemov (ko na primer gre za fitofaške žuželke).
Za številne glive je to ključni encim za nastanek vodikovega peroksida, ki spodbuja razgradnjo lignina. Za drugo vrsto gliv je zgolj antibakterijski in protiglivični obrambni sistem.
Funkcije v industriji
Na industrijskem področju je bila glukoza oksidaza izkoriščena na več načinov, med katerimi je mogoče določiti:
- Kot dodatek med predelavo hrane, kjer deluje kot antioksidant, konzervans in stabilizator živilskih izdelkov.
- Pri ohranjanju mlečnih derivatov, kjer deluje kot protimikrobno sredstvo.
- Uporablja se med proizvodnjo jajčnega prahu za izločanje glukoze in proizvodnjo vodikovega peroksida, ki preprečuje rast mikroorganizmov.
- Prav tako ima uporabnost pri proizvodnji nizkih vin v alkoholu. To je posledica njegove sposobnosti porabe glukoze, ki je prisotna v sokovih, ki se uporabljajo za fermentacijo.
Vam lahko služi: laktoferrin: struktura in funkcije- Glukonska kislina, eden od sekundarnih produktov reakcije, ki jo katalizira glukoza oksidaze, se izkorišča tudi za tekstilno obarvanje, čiščenje kovinskih površin, kot dodatek za hrano, kot dodatek v detergentih in celo v zdravilih in kozmetiki.
Senzorji glukoze
Obstaja več testov za cenzuro koncentracije glukoze v različnih pogojih, ki temeljijo na imobilizaciji encima glukoze oksidaze v dani podpori.
V industriji so zasnovane tri vrste preskusov, ki uporabljajo ta encim kot biosenzor, razlike med njimi.
Poleg uporabnosti v prehrambeni industriji se biosenzorji glukoze izkoristijo za določanje količine glukoze v telesnih tekočinah, kot sta kri in urin. To so ponavadi rutinske študije za odkrivanje patoloških stanj in drugih fizioloških stanj.
Reference
- Bankar, s. B., Bule, m. V, Singhal, R. S., & Ananthanarayan, L. (2009). Glukoza oksidaza - pregled. Napredovanje biotehnologije, 27(4), 489-501.
- Haouz, a., Twist, c., Zentz, c., Tauc, str., & Alpert, b. (1998). Dinamične in strukturne lastnosti encima glukoze oksidaze. Eur Biophys, 27, 19-25.
- Raba, j., & Mottola, h. Do. (devetnajst devetdeset pet). Glukoza oksidaza kot analitični reagent. Kritični pregledi v analitični kemiji, 25(1), 1-42.
- Wilson, r., & Turner, do. (1992). Glukoza oksidaza: idealen encim. Biosenzorji in bioelektronika, 7, 165-185.
- Wong, c. M., Wong, k. H., & Chen, x. D. (2008). Glukoza oksidaza: naravni pojav, funkcija, lastnosti in industrijske aplikacije. Mikrobiol biotehnol, 75, 927-938.

