Ketone Vrste, lastnosti, nomenklatura, uporabe, primeri
- 4087
- 449
- Stuart Armstrong
The ketoni So organske spojine, ki imajo skupino karbonile (-CO). So preproste spojine, v katerih je karbona karbonilne skupine povezana z dvema ogljikovih atomih (in njihovimi nadomestnimi verigami)). Ketoni so "preprosti", ker nimajo reaktivnih skupin, kot sta -oh ali -Cl združeni v ogljik.
Ketoni, prepoznani kot polarni spojine, so običajno topni in nestanovitni, zaradi česar so dobra topila in dodatke za parfume. Poleg tega jih je enostavno pripraviti, razmeroma stabilno in ima visoko reaktivnost, zaradi česar je skoraj popolna vmesna spojina za pripravo bolj zapletenih organskih spojin.
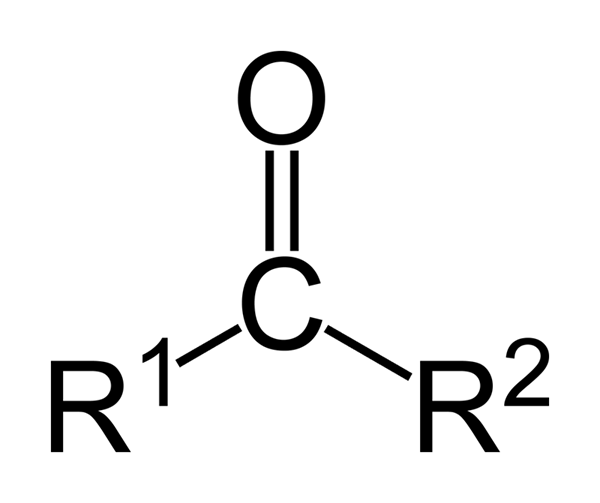
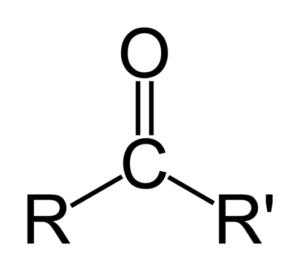
 Splošna formula ketonov
Splošna formula ketonov Končno je izločanje ketonov iz človeškega telesa običajno povezano z nizko raven sladkorja (v primerih diabetika in/ali ekstremnih na tešče), kar lahko bolniku povzroči resne zdravstvene težave.
[TOC]
Splošna formula ketonov
Ketoni so karbonilne spojine, v katerih je ta skupina povezana z dvema skupinama ogljikovodikov; To so lahko alkilne skupine, skupine benzenskih obročev ali oboje.
Keton je mogoče predstaviti preprosto kot r- (c = o) -r ', kjer sta r in r' dve verigi katerega koli ogljikovodika (alko, alkeni, alkini, cikloalkanos, derivati benzena in drugih). Ni ketonov z vodikom, pritrjenim na karbonilno skupino.
Obstaja široko paleto metod za pripravo ketonov na industrijskem in laboratorijskem področju; Poleg tega je pomembno opozoriti, da lahko ketone sintetizirajo različni organizmi, vključno s človeškimi bitji.
V industriji najpogostejša metoda za sintezo ketonov vključuje oksidacijo ogljikovodikov, običajno z uporabo zraka. V majhnem obsegu se ketoni običajno pripravijo z oksidacijo sekundarnih alkoholov, kar daje cetoni in vodni izdelki kot izdelki.
Poleg teh najpogostejših metod lahko ketone sintetiziramo skozi alkene, alkine, soli dušikovih spojin, estrov in številne druge spojine, zaradi česar jih je enostavno pridobiti.
Vrste ketonov
Za ketone obstaja več klasifikacij, odvisno predvsem od substituentov v njihovih R verigah. Spodaj so imenovane najpogostejše klasifikacije za te snovi:
Glede na strukturo njene verige
V tem primeru je keton razvrščen tako, da je strukturirana njegova veriga: alifatski ketoni so tisti, ki imajo dva R in R radikala, ki imata alkilno radikalno obliko (alkani, alkeni, alkini in cikloalkanos).
Lahko vam služi: izoamilni alkohol: struktura, lastnosti, uporabe in tveganjaPo drugi strani so aromatični tisti, ki tvorijo derivati benzena, medtem ko so še vedno ketoni. Končno so mešani ketoni tisti, ki imajo alkilično in radikalno r 'aril ali obratno.
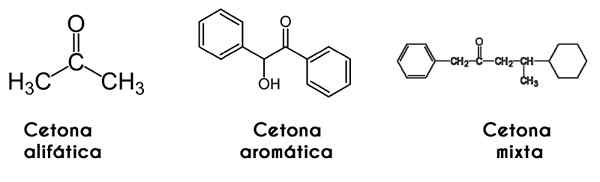 Od leve proti desni: propanona, benzofrona in fenilmetilbutanone. Slike Wikimedia Commons.
Od leve proti desni: propanona, benzofrona in fenilmetilbutanone. Slike Wikimedia Commons. Glede na simetrijo njihovih radikalov
V tem primeru Radikale R in R preučujejo karbonilno skupino; Kadar so te enake (enake), se keton imenuje simetričen; Ko pa so drugačni (kot večina ketonov), se imenuje asimetrično.
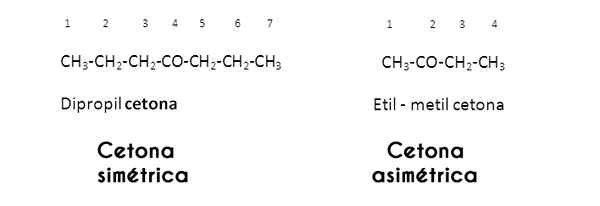 Slike prek Wikimedia Commons.
Slike prek Wikimedia Commons. Glede na nasičenost svojih radikalov
Ketone lahko razvrstimo tudi v skladu z nasičenostjo njihovih ogljikovih verig; Če so ti v obliki alkanov, keton sebe pokliče nasičen keton. Po drugi strani pa, če so verige podobne alkeni ali alkini, se keton imenuje nenasičen keton.
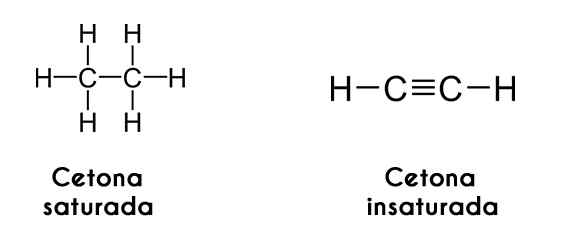 Na levi strani acetilen desno. Slike prek Wikimedia Commons.
Na levi strani acetilen desno. Slike prek Wikimedia Commons. Dicetoni
To je razred, razen Cetone, saj imajo verige tega ketona dve karbonilni skupini v svoji strukturi. Nekateri od teh ketonov imajo edinstvene značilnosti, na primer večjo dolžino povezav med ogljikovimi.
Na primer, dicetoni, pridobljeni iz cikloheksana.
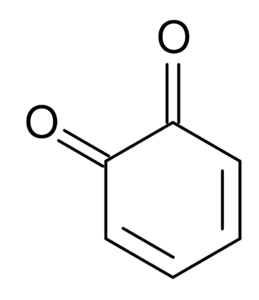 Ortho-Benzoquinon. Jug pri angleški Wikipediji / javni domeni
Ortho-Benzoquinon. Jug pri angleški Wikipediji / javni domeni Fizikalne in kemijske lastnosti ketonov
Ketoni so, tako kot večina aldehidos. Njene lastnosti so opisane spodaj:
Vrelišče
Ketoni so zelo hlapni, znatno polarni in ne morejo darovati vodikov za vodikove vezi (nimajo atomov vodika, vezanih na svojo karbonilno skupino), zato imajo višje vrelišča kot alkeni in ethers, vendar nižji od alkoholov iste molekulske mase.
Vrelišča ketona se poveča, ko se velikost molekule povečuje. To je posledica intervencije sil van der Waals in Dipolo-Dipolo, ki potrebujejo večjo količino energije za ločitev privlačnih atomov in elektronov znotraj molekule.
Topnost
Topnost ketonov močno vpliva na del sposobnosti teh molekul, da sprejmejo vodike v njihovem kisikovem atomu in tako tvorijo vodikovo vez z vodo. Poleg tega so sile privlačnosti, disperzije in dipol-dipola med ketoni in vodo, ki povečujejo njihov topni učinek.
Vam lahko služi: železo (element): značilnosti, kemična struktura, uporabaKetoni izgubijo zmogljivost topnosti, večja je njihova molekula, saj začnejo zahtevati več energije, da se raztopijo v vodi. So topni tudi v organskih spojinah.
Kislost
Zahvaljujoč svoji karbonilni skupini imajo ketoni kisle naravo; To se zgodi zaradi zmogljivosti resonance, ki jo ima ta funkcionalna skupina, kar lahko da protone svoje dvojne vezi, da tvori konjugirano bazo, imenovano Enol.
Reaktivnost
Ketoni so del velikega števila organskih reakcij; To se pojavi zaradi dovzetnosti njegovega karbonilnega ogljika proti nukleofilnemu dodajanju, poleg polarnosti tega.
Kot je navedeno zgoraj, veliko reaktivnost ketonov izdeluje priznani vmesni izdelek, ki služi kot osnova za sintezo drugih spojin.
Nomenklatura
Ketoni so imenovani v skladu s prednostno nalogo ali pomembnostjo karbonilne skupine v celotni molekuli, tako da, ko imate molekulo, ki jo ureja karbonilna skupina, je keton poimenovan tako.
Kot glavna veriga je večja dolžina, ki jo ima karbonilna skupina, nato pa je molekula poimenovana. Če karbonilna skupina nima prednosti pred drugimi funkcionalnimi skupinami molekule, jo identificiramo z "-oxo".
Za bolj zapletene ketone je mogoče položaj funkcionalne skupine identificirati s številom, v primeru dicetonov (ketone z dvema substituentama r in r 'identičnim) pa je molekula poimenovana s pripono "-diona".
Končno lahko besedo "Cetona" uporabimo tudi po identifikaciji radikalnih verig, povezanih s karbonilno funkcionalno skupino.
Razlika med aldehido in ketoni
Največja razlika med aldehidi in ketoni je prisotnost vodikovega atoma, pritrjenega na karbonilno skupino v aldehidih.
Ta atom ima pomemben učinek, ko gre za vključitev molekule v oksidacijsko reakcijo: aldehid bo tvoril karboksilno kislino ali sol karboksilne kisline, odvisno od tega, ali se oksidacija pojavi v kislini ali osnovnih pogojih.
Po drugi strani Cetona nima tega vodika, zato se najmanjši koraki, potrebni za oksidacijo.
Obstajajo metode za oksidacijo ketona (z oksidacijskimi sredstvi veliko močnejši od tistih, ki se običajno uporabljajo), vendar razbijejo cetonsko molekulo in jo najprej ločijo na dva ali več delov.
Vam lahko služi: ionizacija v fiziki in kemiji: koncept, proces in primeriIndustrijska in vsakdanje življenje
V panogi opazimo ketone v parfumih in slikah, pri čemer jemljemo stabilizacijske in kondomi papirje, ki preprečujejo, da bi se druge sestavine mešanice razgradile; Prav tako imajo širok spekter kot topila v tistih panogah, ki poleg farmacevtske izdelke proizvajajo eksplozive, slike in tekstil.
Aceton (najmanjši in manjši keton) je zelo dobro prepoznan svet topila.
V naravi se lahko ketoni pojavijo kot sladkorji, imenovani ketusi. Ketosi so monosaharidi, ki vsebujejo cetono po molekuli. Najbolj znana ketoza je fruktoza, sladkor, ki ga najdemo v sadju in medu.
Z delovanjem ketonov se pojavi tudi biosinteza maščobnih kislin, ki se pojavljajo znotraj citoplazme živalskih celic. Končno, in kot že omenjeno, lahko pride do dviga ketonov v krvi po tesnem ali v primerih sladkorne bolezni.
Primeri ketonov
Butanona (C4H8Da)
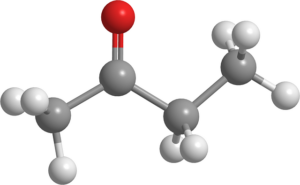 Butanonska molekula. Vir: Pixabay.
Butanonska molekula. Vir: Pixabay. Ta tekočina, znana tudi kot MEK (ali MEC), nastaja v velikem obsegu v industriji in se uporablja kot topilo.
Cikloheksanon (c6H10Da)
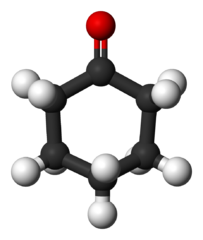 Molekula cikloheksanona. Benjah-bmm27 / javna domena
Molekula cikloheksanona. Benjah-bmm27 / javna domena Ta keton, proizveden v velikem obsegu, se uporablja kot predhodnik najlonskega sintetičnega materiala.
Testosteron (c19H22Tudi2)
 Molekula testosterona. Wikimedia Commons
Molekula testosterona. Wikimedia Commons To je glavni hormon moškega spola in anaboličnega steroida, ki ga najdemo pri večini vretenčarjev.
Progesteron (cenaindvajsetH30Tudi2)
 Medroxiprogesteron acetat, ciklofem komponenta
Medroxiprogesteron acetat, ciklofem komponenta Endogeni steroidni in spolni hormon, ki sodelujejo v menstrualnem ciklu, nosečnosti in embriogenezi pri ljudeh in drugih vrstah.
Aceton (Pogl3(Co) ch3)
 Acetonska spojina. Benjah-bmm27 / javna domena
Acetonska spojina. Benjah-bmm27 / javna domena Znan tudi kot propanona, je brezbarvna spojina, ki se uporablja za proizvodnjo različnih industrijskih izdelkov, kot je plastika, pa tudi za higienske izdelke in kozmetike, kot je odstranjevanje.
Kortizon (cenaindvajsetH28Tudi5)
 Kortizon. Benjah-bmm27 / javna domena
Kortizon. Benjah-bmm27 / javna domena Steroidni hormon, ki se uporablja za boj proti določenim težavam in stanji, kot so vnetja, akne, alergije in druge vrste kožnih reakcij, astma ali rak in levkemija.
Benzofenona (c13H10Da)
 Benzofenom. Benjah-bmm27 / javna domena
Benzofenom. Benjah-bmm27 / javna domena Spojina, ki se pogosto uporablja pri ustvarjanju parfumov in drugih kozmetičnih ali sončnih izdelkov zaradi svoje aromatične sestave.
Reference
- Wikipedija. (s.F.). Keton. Pridobljeno iz in.Wikipedija.org
- Britannica, e. (s.F.). Keton. Pridobljeno od Britannice.com
- Univerza, m. S. (s.F.). Aldehidi in ketoni. Pridobljeno iz kemije.MSU.Edu
- Chemguide. (s.F.). Uvod aldehidi in ketoni. Pridobljeno iz ChemGuide.co.Združeno kraljestvo
- Calgary, u. Tudi. (s.F.). Ketoni. Pridobljeno iz kem.Ucalgary.AC

