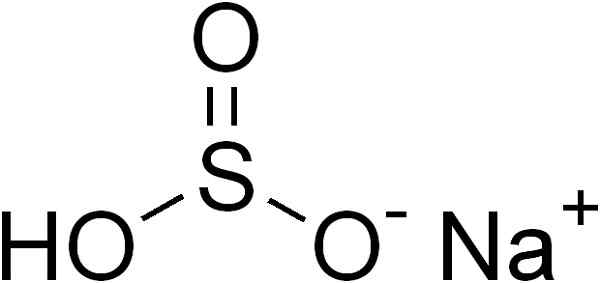
Struktura natrijevega bisulfita (NAHSO3), lastnosti, uporabe, pridobivanje
- 3839
- 700
- Miguel Gutmann DVM
On natrijev bisulfit Gre za anorgansko trdno snov, ki jo tvori ionski natrij NA+ in hso bisulfitni ion3-. Njegova kemična formula je nahso3. Je kristalna bela trdna trdna in za svoje antioksidativne lastnosti se pogosto uporablja kot konzervans za hrano (na primer pri nekaterih džemih).
Nahso3 Gre za zmanjšanje kemične spojine, ki je nasprotno od oksidacije, zato v mnogih svojih aplikacijah deluje kot antioksidant, kot so užitni izdelki, saj preprečuje njegovo poslabšanje.
 Nekateri komercialni zastoji vsebujejo nahso natrijev bisulfit3. Avtor: OpenCLIPART-VEKTORJI. Vir: Pixabay.
Nekateri komercialni zastoji vsebujejo nahso natrijev bisulfit3. Avtor: OpenCLIPART-VEKTORJI. Vir: Pixabay. Vendar je bila ta uporaba vprašljiva, ker so pri ljudeh poročali o primerih astme, potem ko so pojedli hrano, ki vsebuje natrijev bisulfit. Pravijo celo, da uniči vitamin B1 od njih.
Mednarodne zdravstvene organizacije so omejile njihovo uporabo na mikrokonntičnosti v hrani.
Vendar ima natrijev bisulfit številne druge uporabe, na primer pri pridobivanju joda, kot proti -okužbe, za beljenje tkiv, za prebavo lesa med pripravo papirnate kaše kot razkužila piva in vinskih sodov itd.
[TOC]
Kemična struktura
Natrijev bisulfit tvori natrijev na kation+ in hSo bisulfitni anion3-.
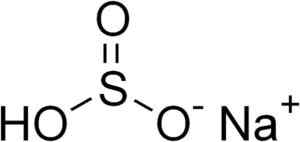 Kemična struktura natrijevega bisulfita3. Edgar181 [javna domena]. Vir: Wikimedia Commons.
Kemična struktura natrijevega bisulfita3. Edgar181 [javna domena]. Vir: Wikimedia Commons. V vodnih raztopinah bisulfit tvori 4 vrste. V razredčeni raztopini je ravnovesje med spodnjimi strukturami:
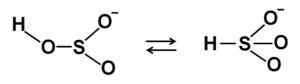 HSO bisulfitne ionske strukture3- V razredčeni vodni raztopini. Avtor: Marilú Stea.
HSO bisulfitne ionske strukture3- V razredčeni vodni raztopini. Avtor: Marilú Stea. Ko koncentracija poveča dve bisulfitni molekuli medsebojno medsebojno, ki tvorita pirosulfitni ion S2Tudi52-:
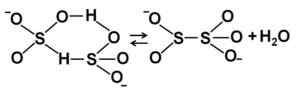 Bisulfitne ionske strukture v koncentrirani vodni raztopini. Avtor: Marilú Stea.
Bisulfitne ionske strukture v koncentrirani vodni raztopini. Avtor: Marilú Stea. Nomenklatura
-Natrijev bisulfit
-Natrijev hidrogenosulfit
-Natrijev hidrosulfit.
Lastnosti
Fizično stanje
Kristalno bela trdna trdna snov.
Molekularna teža
104,06 g/mol
Tališče
Razpade.
Gostota
1,48 g/cm3 pri 20 ° C.
Topnost
Voda topna: 29 g/100 g vode.
ph
Njegove raztopine so kisle, s pH med 2,5 in 5,5.
Kemične lastnosti
V vodni raztopini natrijevega bisulfita3 je ločen v svoje ione: natrijev kation Na+ in hSo bisulfitni anion3-.
Če je natrijev bisulfit izpostavljen zraku2 in počasi oksidira sulfat2SW4.
Lahko vam služi: galna kislina: struktura, lastnosti, pridobivanje, uporabeČe se segreje, dokler njegova razgradnja ne oddaja žveplovih oksidov in natrijevega monoksida.
Je reducirajoče sredstvo, ki je nasprotno od oksidanta. In zaradi tega se lahko obnaša kot antioksidant.
Ima rahel vonj po žveplom. Ni vnetljivo.
Tveganja
Nahso natrijev bisulfit3 To je močno usnje in tkivo, ki draži. Prah draži oči, nos in grlo. Z zaužitjem draži želodec. Veliki odmerki lahko povzročijo nasilne krče, drisko, depresijo in smrt.
Ni gorivo, vendar je ogrevano, da nastanejo dražilni in strupeni plini.
Pridobivanje
Pripravimo ga z nasičenjem raztopine natrijevega karbonata na2Co3 Z žveplovim dioksidom tako2 in kristalizira v raztopini.
Prijave
V industriji celuloze in papirja
Nahso3 Uporablja se pri prebavi lesa, tako da lahko nato postane papir. Služi tudi kot belp celuloze.
Uporablja se tudi za odpravljanje klora, ko je papirna celuloza s tem beljena.
V živilski industriji
Natrijev bisulfit za njegovo zmanjšanje premoženja deluje kot antioksidant.
Uporablja se kot konzervans v veliki količini hrane in pijač, vključno z vinom in pivom, da se prepreči njegovo poslabšanje in izboljša okus.
Služi za beljenje hrane, kot so določeni užitni škrobi.
Zmanjšuje ali preprečuje poslabšanje hrane, omogoča pogoj testa, ki se uporablja v pečeni hrani in se med mokrimi mletje mehča za mehčanje koruznih zrn.
Poleg nadzora fermentacije vina in piva deluje kot antiseptik v svoji izdelavi, ker služi kot sterilizacijo in fungicid v sodih in zobnikih.
 Vinski ali pivski sodi včasih razkužemo z natrijevim bisulfitom3. Avtor: Clker-brez vektorjev. Vir: Pixabay.
Vinski ali pivski sodi včasih razkužemo z natrijevim bisulfitom3. Avtor: Clker-brez vektorjev. Vir: Pixabay. V posušenem sadju je v koncentracijah nad 100 ppm (PPM pomeni "deli na milijon"), v mnogih drugih živilih je v koncentracijah med 10 in 100 ppm, kot so zamrznjen in suh krompir, kumarice, omake in marmeladi.
 Komercialna vložena hrana pogosto vsebuje nahso natrijev bisulfit3. Avtor: Fotografska mešanica. Vir: Pixabay.
Komercialna vložena hrana pogosto vsebuje nahso natrijev bisulfit3. Avtor: Fotografska mešanica. Vir: Pixabay. Polemika o njegovi uporabi v hrani
Nekaj skrbi zaradi strupenih učinkov takoj in dolgoročno natrijevega bisulfita v hrani. Obstajajo različna mnenja.
Vam lahko postreže: kalijev ferocianidObstajajo poročila o neželenih učinkih bolnikov z astmo, ki je dihala, po zaužitju živil z Nahso3. Drugi viri kažejo, da bisulfitni ion lahko uniči vitamin B1 ali tiamin.
 Dekle si prizadeva za lajšanje astme. Avtor: OpenCLIPART-VEKTORJI. Vir: Pixabay.
Dekle si prizadeva za lajšanje astme. Avtor: OpenCLIPART-VEKTORJI. Vir: Pixabay. Vendar so nekateri raziskovalci leta 1985 ugotovili, da natrijev bisulfit služi za zaščito pred kemičnimi sredstvi in zavira ali preprečuje preoblikovanje celic v rak. Nizki odmerki so najboljši.
Ta zaščitni učinek je bil razložen na podlagi njegovih lastnosti zmanjševanja ali antioksidantov in na ta način bi lahko napadel proste radikale.
Po drugi strani Svetovna zdravstvena organizacija ali WHO (za njen kratica za angleščino Svetovna zdravstvena organizacija), priporoča kot sprejemljivo raven dnevnega vnosa približno 0,7 mg/kg osebe.
To pomeni, da je priporočljivo, da tega zneska ne presežete.
Uprava za prehrano in medicino ZDA ali USFDA (angleška kratica Ameriška uprava za hrano in zdravila), je razvrstil natrijev bisulfit kot "splošno priznan kot zavarovanje".
V kmetijskih aplikacijah
Uporablja se pri nizkih koncentracijah NAHSO3 Služi kot regulator rasti rastlin, za izboljšanje fotosinteze in spodbujanje uspešnosti pridelka.
Ta cilj je bil preizkušen v različnih vrstah rastlin, kot so jagode in čajne rastline.
 Jagodne rastline izboljšajo svoje zmogljivosti z majhnimi količinami Nahso3 V namakalni vodi. Avtor: Alyssapy. Vir: Pixabay.
Jagodne rastline izboljšajo svoje zmogljivosti z majhnimi količinami Nahso3 V namakalni vodi. Avtor: Alyssapy. Vir: Pixabay. Je aktivna sestavina številnih pesticidov in biocidov.
V vodnih okoljih lahko tudi pospeši preoblikovanje nekaterih herbicidov v manj strupene izdelke z odpravo klora.
Pri pridobivanju joda
Nahso3 To je reducirajoča spojina, ki se uporablja za sproščanje jodinusa natrijevega naio3. To je eden izmed načinov, kako jod pridobiti iz virov, kot so čilski nitro ali nekatere vode Salinas.
Po kristalizaciji natrijevega nitrata nitratne raztopine bruto Čila obstaja raztopina NAIO3 ki se zdravi z natrijevim bisulfitom3, ustvarjanje prostega joda.
2 NAIO3 + 5 NaHSO3 → 3 NaHSO4 + Na2SW4 + Yo2
V industriji pohištva in lesa
Nahso3 Preizkušena je bila za spreminjanje sojinih beljakovin in izboljšanje njenih oprijemljivih lastnosti z lesom z namenom, da se koščki lesa med seboj pripravijo na primer aglomerate, leseni karton ali kamnito karton, pult v obliki itd. Vse za pohištvo ali deske, med več aplikacijami.
Lahko vam služi: litijev hidroksid (LIOH) Aglomerat drobtin ali lesenih ostankov. Avtor: Titus tschardke [javna domena]. Vir: Wikimedia Commons.
Aglomerat drobtin ali lesenih ostankov. Avtor: Titus tschardke [javna domena]. Vir: Wikimedia Commons. To se naredi za nadomeščanje tradicionalnih lepil, ki temeljijo na formaldehidu, ker tako v njihovem proizvodnem procesu kot med uporabo ponavadi svobodno formalizirajo atmosfero, ki je strupena spojina.
Natrijev bisulfit izboljšuje trdno vsebnost sojinega beljakovinskega lepila in zmanjšuje viskoznost tega izboljšanja njegove pretočnosti, tako da prodira po poreh lesa, s tem pa poveča svojo kohezijo in med koščki.
Sojino beljakovinsko lepilo, spremenjeno z nahso3 Ima dobro odpornost na vodo in odlično stabilnost shranjevanja zaradi antioksidantnega delovanja natrijevega bisulfita.
To potrjuje, da so spremenjeni sojini beljakovinski lepili z Nahso3 So primerljivi z lepili, ki temeljijo na formaldehidu in jih je mogoče uporabiti v pohištvu in leseni industriji, manj onesnažujejo.
V različnih aplikacijah
Ima več načinov uporabe, na splošno na podlagi njegovih reducirajočih lastnosti (kar je nasprotno od oksidanta). Tu je nekaj aplikacij.
-V fotografiji.
-V usnjenem tangu, da odstranite lase s kože.
-Terapevtske uporabe: proti -infektivno. Uporablja se kot antioksidant v nekaj kapljicah za -ojos.
-Pri ekstrakciji zemeljskega plina s hidravličnim zlomom.
-Pri barvanju vlaken se uporablja za pripravo vročih ali hladnih kad, za solubilizacijo nekaterih barvil ali barvil.
-Kot zmanjšanje perila ali beljenja za beljenje volne, svile in rastlinskih vlaken.
-V kemijskih laboratorijih za odstranjevanje madežev kože in oblačil. V biokemijskih laboratorijih kot konzervans ali rešitve tekočine, ki jih je mogoče sčasoma poslabšati. Kot kemični reagent.
-Za gumijasto koagulacijo lateksa.
-V kozmetični industriji kot antioksidant.
-Razkužilo in belilo.
-Pri čiščenju odpadne vode za odpravo klora, ki se uporablja v zadnji fazi dezinfekcije, in biti sposoben prenesti vode, ki so že obdelane v okolje.
 Natrijev bisulfitni rezervoar v čistilni napravi v Kaliforniji, kjer se uporablja za odpravo presežka klora, preden se prečiščene vode prenesejo v okolje. Grendelkhan [cc by-sa 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]. Vir: Wikimedia Commons.
Natrijev bisulfitni rezervoar v čistilni napravi v Kaliforniji, kjer se uporablja za odpravo presežka klora, preden se prečiščene vode prenesejo v okolje. Grendelkhan [cc by-sa 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]. Vir: Wikimedia Commons. Reference
- Ali.S. Nacionalna knjižnica medicine. (2019). Natrijev bisulfit. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Qi, g. et al. (2013). Adhezija in fizikalno -kemijske lastnosti Ser proteina, spremenjene z natrijevim bisulfitom. J Am Oil Chem Soc (2013) 90: 1917-1926. Okreval od AOC.Spletna knjižnica.Wiley.com.
- Borek, c. et al. (1985). Natrijev bisulfit ščiti pred radiogogeno in kemično inducirano transformacijo v celicah hrčka in mišjih C3H/10T-1/2. Toxicol Ind Health 1985sep; 1 (1): 69–74. Okreval iz revij.Sagepub.com.
- Friedler, npr. et al. (2015). Nenehni aktivni pristop spremljanja za prepoznavanje navzkrižnih povezav med pitno vodo in sistemi za distribucijo odpadkov. Okolje Monit Asses (2015) 187: 131. Povezava je bila obnovljena.Springer.com.
- Bombaž, f. Albert in Wilkinson, Geoffrey. (1980). Napredna anorganska kemija. Četrta izdaja. John Wiley & Sons.
- Sunnyvale Cleanwater Program. (2019). Glavni načrt za nadzor onesnaževanja vode. Okrevano iz Sunnyvaleclecleanwater.com.
- Barros Santos, c. (2008). Aditivi pri hranjenju Špancev in zakonodaji, ki urejajo njihovo dovoljenje in uporabo. Knjige Vizija. Okrevano iz knjig.Google.co.pojdi.

